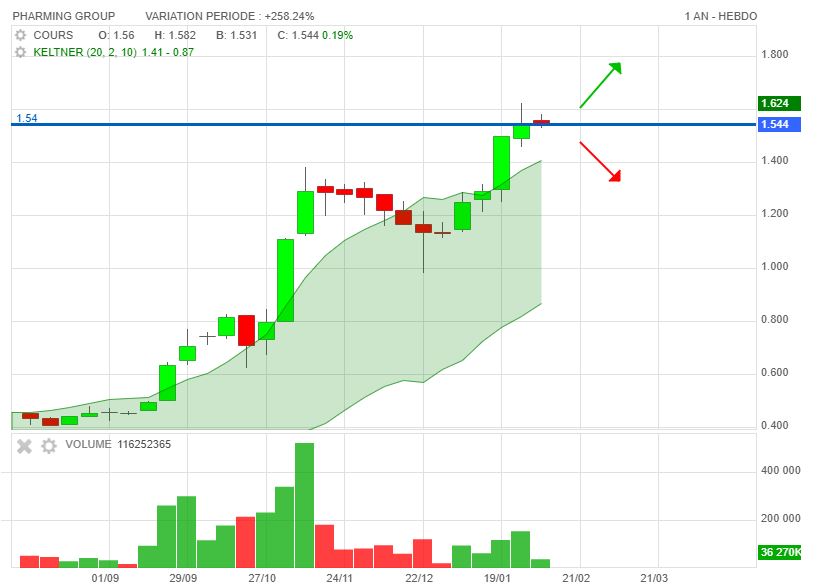
1,60/1,62 signal haussier le plus vraissemblble.
1,48 signal baissier.
|
Répondre
|
Il aurait fallu entrer à 20 ou 30 centimes quand Toto le disait.
Il fallait la surveiller il y a 6 mois, en fait.
On peut toujours entrer sur repli avec un objectif 1.80 ou 2 euro.
|
Répondre
|
|
Répondre
|
|
Répondre
|
|
Répondre
|
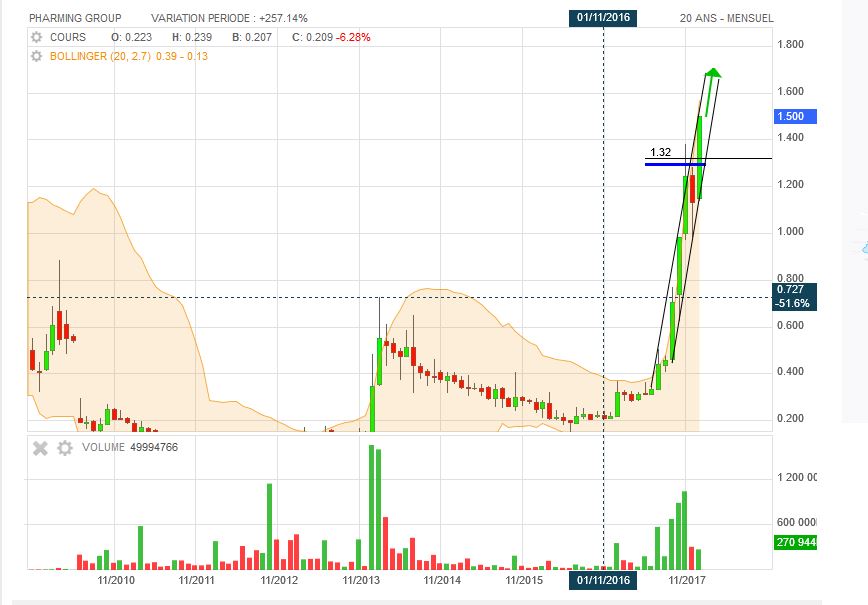
Serait pas un peu derrière la hausse conséquente ???
1.50 EUR 14,24%
|
Répondre
|
Message complété le 19/01/2018 17:00:54 par son auteur.
+10,21% à 1,447
|
Répondre
|
Message complété le 19/01/2018 14:15:15 par son auteur.
1,386 EUR +5,56% le plus haut sur un an dépassé.
|
Répondre
|
|
Répondre
|
|
Répondre
|
|
Répondre
|
|
Répondre
|
La hausse est loin d'être derrière nous, pour ça il faut connaitre le dossier ;)
Achat à 0,42 et toujours confiant pour la suite. Je vise au moins 2€ cette année.
|
Répondre
|
N, Netherlands, January 17, 2018 /PRNewswire/ --
Pharming Group N.V. ("Pharming" or "the Company") (Euronext Amsterdam: PHARM) announced today that the U.S. Food and Drug Administration (FDA) has accepted for review Pharming's supplemental Biologics License Application (sBLA) for RUCONEST[Recombinant Human C1 Esterase Inhibitor/ conestat alfa] for routine prophylaxis to prevent attacks in adult and adolescent patients with hereditary angioedema (HAE). The FDA has indicated that the sBLA is sufficiently complete to permit a substantive review and has set an action date of September 21, 2018.
N, Pays-Bas, 17 janvier 2018 / PRNewswire / -
Pharming Group NV («Pharming» ou «la Société») (Euronext Amsterdam: PHARM) a annoncé aujourd'hui que la Food and Drug Administration des États-Unis (FDA) a accepté de réviser la demande de licence complémentaire biologique de Pharming (sBLA) pour RUCONEST [recombinante humaine C1 estérase Inhibitor / conestat alfa] pour la prophylaxie de routine afin de prévenir les crises chez les adultes et les adolescents atteints d'angio-œdème héréditaire (AOH). La FDA a indiqué que le sBLA est suffisamment complet pour permettre un examen de fond et a fixé une date d'action au 21 septembre 2018.
|
Répondre
|
Message complété le 17/01/2018 08:04:24 par son auteur.
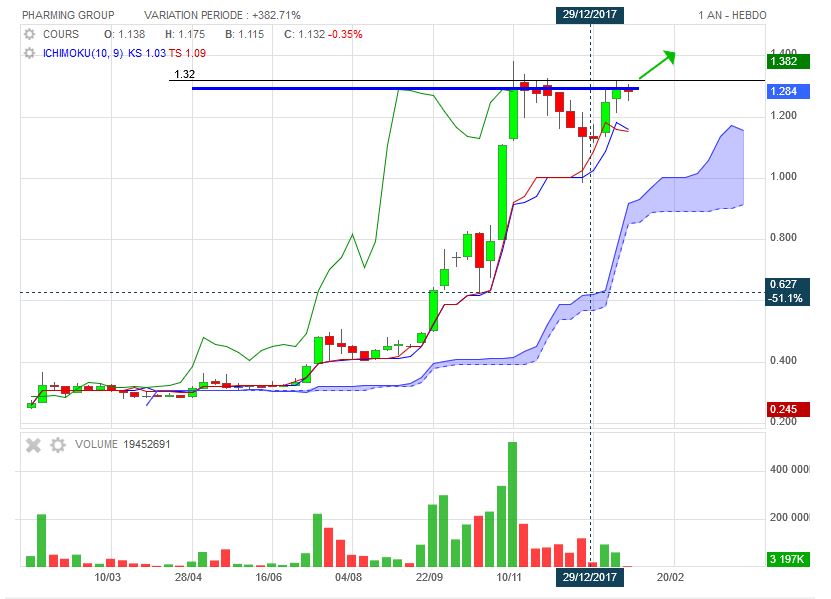
Échec hier sur la résistance 1,31 et clôture 1,291 +1,65%. Nouveau test aujourd'hui avec communiquer FDA.
N, Netherlands, January 17, 2018 /PRNewswire/ --
Pharming Group N.V. ("Pharming" or "the Company") (Euronext Amsterdam: PHARM) announced today that the U.S. Food and Drug Administration (FDA) has accepted for review Pharming's supplemental Biologics License Application (sBLA) for RUCONEST[Recombinant Human C1 Esterase Inhibitor/ conestat alfa] for routine prophylaxis to prevent attacks in adult and adolescent patients with hereditary angioedema (HAE). The FDA has indicated that the sBLA is sufficiently complete to permit a substantive review and has set an action date of September 21, 2018.
N, Pays-Bas, 17 janvier 2018 / PRNewswire / -
Pharming Group NV («Pharming» ou «la Société») (Euronext Amsterdam: PHARM) a annoncé aujourd'hui que la Food and Drug Administration des États-Unis (FDA) a accepté de réviser la demande de licence complémentaire biologique de Pharming (sBLA) pour RUCONEST [recombinante humaine C1 estérase Inhibitor / conestat alfa] pour la prophylaxie de routine afin de prévenir les crises chez les adultes et les adolescents atteints d'angio-œdème héréditaire (AOH). La FDA a indiqué que le sBLA est suffisamment complet pour permettre un examen de fond et a fixé une date d'action au 21 septembre 2018.
|
Répondre
|
Serait pas un peu derrière la hausse conséquente ???
|
Répondre
|
|
Répondre
|

 Suivez les marchés avec des outils de pros !
Suivez les marchés avec des outils de pros !