Valneva: contrôle direct des ventes d'Ixiaro aux Etats-Unis. - Page 3
Cours temps réel: 3,588 -3,55%| Cours | Graphes | News | Analyses et conseils | Société | Historiques | Vie du titre | Secteur | Forum |
Bill ,ne lis pas entre les lignes cela concerne énormément de Pays.
|
Répondre
|
Pour rappel Bill17, faut lire ce qui est écrit dans le compte rendu de ce matin sur le T1 ...
Il est écrit : "Le marché mondial total des vaccins contre le chikungunya vaccines est estimé à plus de $500 millions19 et le marché du voyage à environ $250 millions.
La société dont le vaccin contre le chikugununya recevra la première autorisation de mise sur le marché aux Etats-Unis sera éligible à l’obtention d’un bon d’évaluation prioritaire (Priority Review Voucher)."
|
Répondre
|
 1
1
Sans esprit de polémique, le vaccin contre le chikungunya ne concerne que quelques habitants de l'ile de la Réunion me semble t'il?
Message complété le 08/05/2020 09:30:03 par son auteur.
merci pour tes précisions Gars d'ain, n'étant pas actionnaire je ne faisait qu’émettre un avis, sans plus.
Bonne journée à toi
|
Répondre
|
Valneva continue d'avancer !...
Valneva va s’allier avec l’Institut Butantan pour son vaccin à dose unique contre le chikungunya dans les pays à revenus faibles et intermédiaires
May 05, 2020 11:45 ET | Source: VALNEVA
Saint-Herblain (France), Sao Paulo, (Brésil), 5 mai 2020 – Valneva SE (« Valneva » ou « le Groupe », société spécialisée dans les vaccins, et l’Institut Butantan, fabricant de produits immunobiologiques, ont annoncé aujourd’hui la signature d’une lettre d’intention liante (binding term sheet) pour le développement, la production et la commercialisation du candidat vaccin à dose unique de Valneva contre le chikungunya, VLA1553, dans les pays à revenus faibles et intermédiaires. Cette collaboration s’inscrit dans le cadre du financement de $23,4 millions que Valneva a reçu de la Coalition pour les Innovations en Préparation aux Epidémies (CEPI) en juillet 2019. Les contrats finaux devraient être signés dans les six prochains mois.
Une fois les contrats finaux signés, Valneva transférera la technologie de son vaccin contre le chikungunya à Butantan, qui développera, produira et commercialisera le vaccin dans les pays à revenus faibles et intermédiaires. Butantan assurera, par ailleurs, certaines études cliniques et études observationnelles de Phase 4 que Valneva utilisera pour répondre à certaines exigences réglementaires. L’accord prévoit de faibles montants à titre de paiement initial et de paiements d’étapes liés au transfert de la technologie.
Valneva a tenu une réunion de fin de Phase 2 avec l’agence de santé américaine FDA en février 2020 et se prépare désormais à initier les essais cliniques de Phase 3 aux Etats-Unis un peu plus tard cette année.
Thomas Lingelbach, Directeur Général de Valneva, a indiqué, “Bien que des millions de personnes aient été infectées par le chikungunya, il n’existe à ce jour aucun vaccin et aucun traitement efficace contre cette très grave maladie. Nous avons hâte de travailler avec l’Institut Butantan pour essayer de mettre fin à ce problème de santé publique et accélérer le développement d’un vaccin contre le chikungunya dans les pays à revenus faibles et intermédiaires, qui sont des zones fortement endémiques."
Dr. Dimas Covas, Directeur de l’Institut Butantan a ajouté, « le fardeau du virus chikungunya ne réside pas seulement dans les deux millions de décès qui ont été enregistrés depuis 2005, mais également dans la persistance chronique des symptômes de la maladie, qui constitue un problème de santé publique de long terme. En relevant le défi de développer, produire et commercialiser le vaccin de Valneva contre le chikugungunya, l’Institut Butantan va renforcer son engagement pour l’amélioration de la santé publique dans les pays à revenus faibles et intermédiaires ».
A propos du chikungunya
Le virus chikungunya (CHIKV) est un alphavirus de la famille des Togaviridae transmis par les moustiques Aedes. Les symptômes cliniques incluent fièvres aigües, douleurs invalidantes aux niveaux des articulations et des muscles ainsi que des maux de tête, nausées et rougeurs, pouvant causer d’importantes séquelles persistantes. Le virus chikungunya provoque une maladie clinique chez 72 à 92% des personnes dans les 4 à 7 jours qui suivent la piqûre d’un moustique infecté2. Les complications résultantes de la maladie incluent des manifestations visuelles, neurologiques, cardiaques et gastro-intestinales ; des décès ont, par ailleurs, été constatés (taux de mortalité entre 0,1% et 4,9% lors des épidémies)1 chez les personnes âgées, plus fragiles. Différentes épidémies de chikungunya ont été rapportées en Asie, en Afrique, en Amérique et, plus récemment (2017), en Europe. Depuis 2017, plus d’un million de cas ont été recensés sur le continent américain3 et l’impact économique de la maladie est considéré comme extrêmement important (ex. l’épidémie de la Colombie en 2014 : $73,6 millions4). Cet impact devrait continuer à s’alourdir alors que les principaux vecteurs du virus (les moustiques Aedes albopictus et Aedes aegypti) ne cessent d’étendre leur territoire. Il n’existe actuellement aucun vaccin préventif, ni traitement efficace contre chikungunya qui est, de ce fait, considéré comme une menace majeure pour la santé publique.
A propos du candidat vaccin de Valneva VLA1553
VLA1553 est un candidat vaccin monovalent vivant atténué contre le chikungunya qui a obtenu le statut de Fast Track de l’autorité de santé américaine « Food and Drug Administration » (FDA) en décembre 20185.
Le candidat vaccin de Valneva a pour objectif d’offrir une protection contre le virus après une seule dose d’immunisation chez l’adulte et l’enfant de plus d’un an. Le vaccin vise une protection de longue durée et un profil d’innocuité comparable à celui des vaccins actuellement commercialisés pour une immunisation active des adultes et des enfants. Les segments démographiques ciblés sont les voyageurs, le personnel militaire, et les populations à risque vivant dans les zones endémiques. Le marché mondial pour des vaccins contre le chikungunya pourrait atteindre 500 millions d’euros par an6, dont un potentiel d’environ $250 millions de dollars sur le marché du voyage.
VLA1553 est basé sur un clone infectieux (CHIKV LR2006-OPY1), atténué par la suppression d’une partie majeure du gène qui encode la protéine complexe réplicase non structurelle nsP3. Il vise à offrir une protection contre plusieurs phylogroupes et souches des épidémies du virus chikungunya7.
A propos de Valneva SE
Valneva est une société spécialisée dans les vaccins contre les maladies générant d’importants besoins médicaux. Le portefeuille de produits de Valneva inclut deux vaccins du voyageur, IXIARO®/JESPECT® contre l’encéphalite japonaise et DUKORAL®8 dans la prévention du choléra et, dans certains pays, de la diarrhée causée par l’ETEC. Le groupe est également propriétaire d’un solide portefeuille de vaccins en développement dont le seul candidat vaccin en phase clinique contre la maladie de Lyme. Valneva compte plus de 500 employés et exerce ses activités depuis l’Autriche, la Suède, la Grande-Bretagne, la France, le Canada et les Etats-Unis. Pour plus d’information, consulter le site internet du Groupe www.valneva.com et suivez la société sur LinkedIn.
A propos de l’Institut Butantan
L’Institut Butantan est le principal fabricant de produits immunobiologiques et de vaccins au Brésil. L’Institut Butantan mène des missions scientifiques au Brésil ainsi qu’à l’étranger par le biais de l’Organisation Pan Américaine de la Santé, de l’Organisation Mondiale de la Santé, de l’UNICEF et des Nations Unies. L’Institut collabore avec d’autres agences du Département de la Santé de l’état de Sao Paulo et du Ministère brésilien de la Santé pour l’amélioration de la santé publique au Brésil. Afin d’atteindre ses objectifs institutionnels, il œuvre en partenariat avec différentes universités et entités comme la Fondation Bill & Melinda Gates. Pour plus d’information, merci de visiter le site internet de l’Institut www.butantan.gov.br ou de contacter le service de presse de l’Institut au (+55 11) 2627-9606 / 9428 ou par courriel à imprensa@butantan.gov.br
A propos de CEPI
CEPI est un partenariat innovant entre organisations publiques, privées, philanthropiques et civiles, lancé au forum économique mondial de Davos en janvier 2017, ayant pour ambition de mettre au point des vaccins contre les maladies à fort potentiel épidémique.
Les maladies ciblées en priorité par CEPI sont le virus Ebola, le virus de Lassa, le MERS-CoV, le virus Nipah, la fièvre de la vallée du Rift et le chikungunya. CEPI investit également dans des plateformes technologiques pouvant être utilisées pour un développement rapide de vaccins contre des pathogènes non-connus (i.e. la maladie X).
CEPI a répondu avec urgence et en coordination avec l’Organisation Mondiale de la Santé à l’émergence du COVID-19. CEPI a initié neuf partenariats pour le développement de vaccins contre ce nouveau coronavirus. Ces programmes s’appuient sur des plateformes déjà soutenus par CEPI ainsi que de nouveaux partenariats. L’objectif est de faire entrer ces candidats vaccins contre le COVID-19 en développement clinique aussi rapidement que possible.
L’engagement de CEPI pour un accès aux vaccins
Comme le COVID-19 le démontre, les maladies infectieuses ignorent les frontières politiques. Nous ne pouvons prévenir ou stopper une menace d’infection mondiale sans avoir un accès équitable aux vaccins dans le monde. CEPI est totalement engagée pour un accès équitable aux vaccins. Cet engagement est le moteur de notre travail. Le soutien de CEPI pour un accès équitable est la clef de notre succès en tant qu’organisation pour la santé mondiale. Un accès équitable aux vaccins - dans le contexte d’une épidémie - signifie que les vaccins permettant de lutter contre cette épidémie doivent d’abord être disponibles pour les populations et dans les lieux où ils sont nécessaires afin de mettre fin à cette épidémie ou contenir cette épidémie, sans tenir compte d’éventuelles capacités financières.
Pour plus d’information, consultez http://www.cepi.net/. Suivez-nous sur @CEPIvaccines.
|
Répondre
|
 0
0
Parfois, il faut savoir lâcher au bon moment.
Ceci n'est qu'un avis, pas une incitation a acheter ou vendre....
**: non actionnaire
|
Répondre
|
@ricoco01 et gars d'ain
Mon pessimisme n'est pas de granit et je serai le premier à me réjouir après avoir été agréablement surpris par les performances de VALNEVA dans quelques semaines ou dans quelques mois.
Bonne soirée
|
Répondre
|
Je pense que Valneva va en surprendre plus d'un d'ici quelques petites semaines.Je la suis depuis des années et je ne vois pas pourquoi une société se positionne sur le rachat d'un vaccin avant même la fin de ses résultats.
|
Répondre
|
VALNEVA a continué de susciter de grands espoirs jusqu'à hier.
Largement déçus et les résultats trimestriels d'hier justement, ne sont pas de nature à engendrer l'enthousiasme … et l'AT n'y changera rien.
Désolé, mais la petite ligne que j'ai renforcée hier ne demande qu'à se réjouir de mon erreur … ERRARE HUMANUM EST PERSEVERARE DIABOLICUM.
Cordialement
|
Répondre
|
C'est quoi ce jargon convenu d'analyste de grande enseigne de bricolage financier : "au vu des résultats trimestriels en demi teintes tout de même ... "
On fait jeu égale avec le T1 / 2019 dans des conditions de marché très défavorables, avec des capacités d'exportation limitées et alors que l'entreprise ne vend quasi plus de vaccins voyage et que les forces armées qui elles aussi sortent moins sont du coup moins besoin de vaccination
Au lieu de ce pipeau gratuit, il convient de saluer l'extrême résistance et solidité des chiffres, dont le T2 bénéficiera en lancé et avec la perception du gros chèque de 135 millions de Pfizer à venir ...
|
Répondre
|
Bonjour,
J'ai bien peur que les excellentes nouvelles aient déjà été intégrées dans le cours de l'action et sanctionnées par les hausses de la fin avril, somme toute assez modestes par rapport à ce que l'on a vu par ailleurs, et dont j'ai pu personnellement profiter.
Mais je ne demande qu'à être convaincu du contraire notamment par … une poussée vigoureuse du cours au vu des résultats trimestriels en demi teintes tout de même ...
|
Répondre
|
 0
0
Pas de problème, patience now!
|
Répondre
|
J'ai l'impression qu'il n'y a pas eu de prise de bénéfice vue le volume.Cela me semble plutôt positif.
|
Répondre
|
Le passage à nouveau des 4€ permettrait d'aller retester la resistance des 4.20! Si celle ci lache, obj 6€
|
Répondre
|
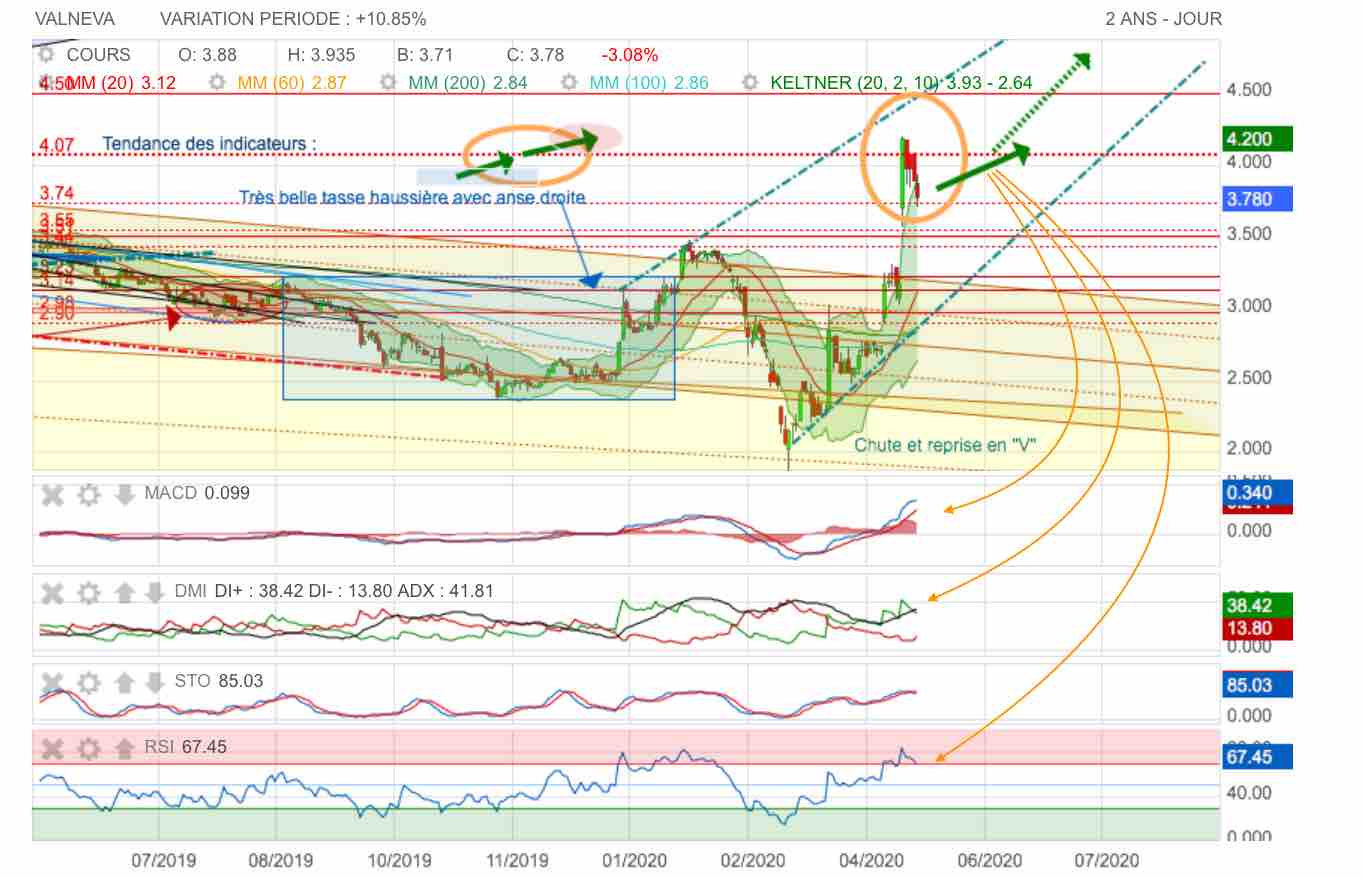
Consolidation latérale de la hausse en cours et réintégration de la keltner haute : la tendance est haussière
Tentative de refroidissement des indicateurs : élimination en cours de la poche spéculative de surachat haussier.
On devrait voir poindre des conseils d'achats compte tenu de l'excellente publication trimestrielle et des moyens dont va disposer Valvena pour booster ses projets avec l'accord Pfizer (voir les posts précédents).
.
|
Répondre
|
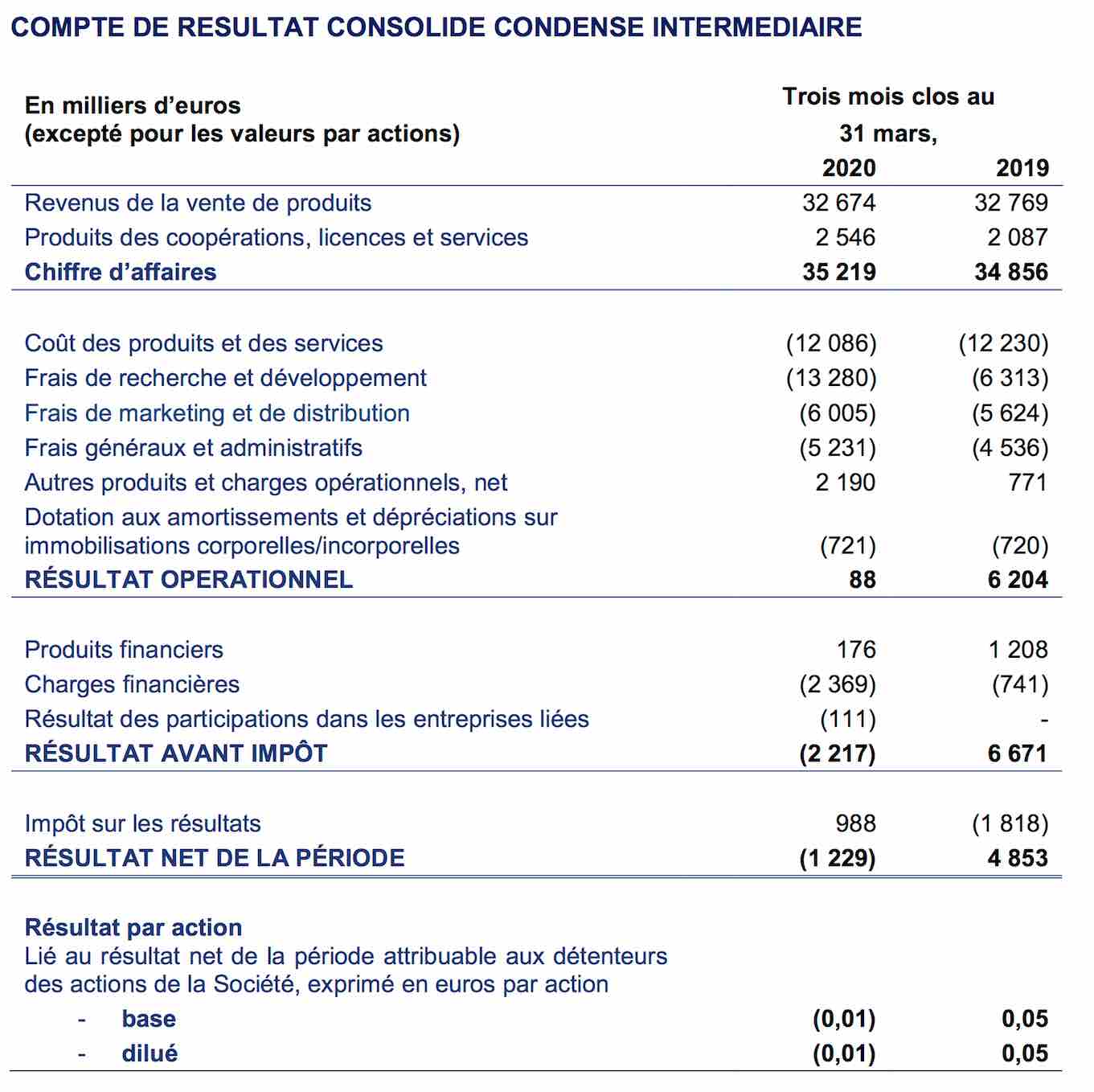
Les résultats annuels sont stables et la différence majeure comptable qui grève le résultats concernant des frais de recherche et développement en hausse de + 6,97 Md'e.
Hors hausse de frais de recherche et développement, le résultat net du trimestre T1 / 2020 aurait été en hausse de +18,23% (+ 0,885Md'e)
Présentation analyste des résultats trimestriels T1 / 2020 [PDF] • 28 pages
https://valneva.com/wp-content/uploads/2020/05/2020_05_07_Valneva_3M_2020_Analyst_Presentation.pdf
Le communiqué de presse COMPLET des comptes figure en post précédent.
Et voici le tableau comptable détaillé du trimestre
https://valneva.com/wp-content/uploads/2020/05/Valneva_Q1_2020_-FS_FR_.pdf
.
|
Répondre
|
Valneva publie ses résultats du premier trimestre et révise ses prévisions 2020 suite à la signature d’un partenariat majeur pour son vaccin Lyme
Communiqué de presse [PDF] | 7 mai 2020
https://valneva.com/wp-content/uploads/2020/05/2020_05_07_VLA_Q1_Results_PR_FR_Final-1.pdf
--------------------------------------------------------------------------------------------------------------
Valneva publie ses résultats du premier trimestre et révise ses prévisions 2020 suite à la signature d’un partenariat majeur pour son vaccin Lyme
Impact limité de la crise du COVID-19 au T1
Partenariat sans précédent signé pour le candidat vaccin de Phase 2 contre la maladie de Lyme
Révision des prévisions 2020 avec notamment une amélioration de l’EBITDA
Initiation du développement d’un vaccin SARS-CoV-2 contre le COVID-19 Résultats financiers solides publiés au T1 2020, impact limité du COVID-19
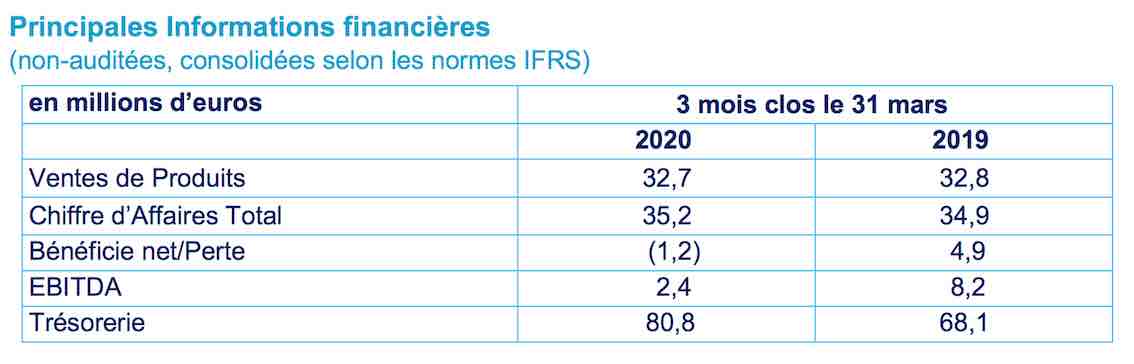
Ventes de produits de €32,7 millions au T1 2020, stables vs T1 2019 (€32,8 millions)
Chiffre d’affaires total de €35,2 millions au T1 2020, stable vs T1 2019 (€34,9 millions)
Marge brute sur les ventes de produits de 69,4% au T1 2020 soutenue par la multiplicité des zones géographiques et la solide performance opérationnelle des sites de production du Groupe
EBITDA1 de €2,4 millions au T1 2020, inférieur à celui du T1 2019 (€8,2 millions) en raison d’une augmentation des investissements de R&D
Flux de trésorerie positifs de €3,0 millions au T1 2020
Solide position de trésorerie de €80,8 millions à fin mars 2020 o soutenueparlerécentaccorddefinancementde$85millionssignéavecdeux fonds d’investissement américains (Valneva n’a effectué à ce jour qu’un tirage de $45 millions dans le cadre de cet accord)
Révision des prévisions 2020 afin de refléter l’impact persistant du COVID-19 et la collaboration pour le vaccin Lyme, intégrant notamment une amélioration de l’EBITDA
Chiffre d’affaires total 2020 désormais estimé entre €95 millions et €135 millions o Cette révision inclut la reconnaissance de €10 millions à €30 millions de revenus provenant de la collaboration sur le candidat vaccin contre la maladie de Lyme, à intégrer aux “autres revenus”2
Prévision pour les autres revenus, hors Lyme, maintenue à environ €10 millions
o Prévision pour les ventes de produits désormais estimée entre €75 millions et €95 millions compte tenu de l’impact persistant de la pandémie de COVID-19
Investissements R&D 2020 estimés à €80 millions au plus, en tenant compte:
o D’un retard potentiel de trois mois pour l’initiation de l’étude de Phase 3 pour le vaccin chikungunya en raison du COVID-19, comme précédemment annoncé
o Des coûts liés au vaccin Lyme dans le cadre de la nouvelle collaboration
o De l’investissement initial du Groupe dans un candidat vaccin contre leSARS-CoV- 2 (VLA2001)
Valneva prévoit désormais pour 2020 un EBITDA négatif de €10 millions à €30 millions, moins important que sa prévision initiale d’un EBITDA négatif d’un maximum de €50 millions en 2020
o Des mesures de réduction des coûts sont par ailleurs mises en œuvre au sein du Groupe et des mécanismes de soutien gouvernementaux sont également utilisés lorsque cela est possible
==================================
Avancées significatives annoncées pour les différents programmes R&D du Groupe depuis le début de l’année
• Signature d’une collaboration sans précédent avec Pfizer pour le candidat vaccin contre la maladie de Lyme VLA153
o Paiement initial de $130 millions et paiements d’étape de $35 millions liés à l’avancée du développement du produit
o Jusqu’à $143 millions de paiements additionnels liés aux premières étapes de commercialisation du produit
o Redevances croissantes sur les ventes, avec un taux débutant à 19%
• Aucun changement de calendrier pour les essais de Phase 2 de VLA15 actuellement en cours, malgré la pandémie de COVID-19. Premiers résultats de Phase 2 toujours attendus en juillet 2020
• Réunion de fin de Phase 2 positive octroyée par la FDA pour le candidat vaccin contre le chikungunya VLA15534
• Initiation de la Phase 3 du vaccin chikungunya dès que la situation liée au COVID-19 le permettra (actuellement prévue pour le T4 2020)
• Initiation de VLA2001 – programme de développement d’un vaccin SARS-CoV-2 contre le COVID-19
o Collaboration avec Dynavax s’appuyant sur les compétences techniques de Valneva et une plateforme existante pour développer un candidat vaccin inactivé et adjuvanté contre le coronavirus
o Utilisation des capacités de laboratoire existantes d’un niveau 3 de biosécurité pour mener les activités précliniques
o Ressources provenant d’autres projets (en tout début de développement) réallouées pour ce programme; recherche de subventions pour financer le développement clinique et les investissements de fabrication.
o Valneva et Dynavax vont travailler de concert avec les autorités réglementaires pour s’accorder sur la stratégie optimale pour un développement clinique accéléré, avec pour objectif d’initier des essais cliniques avant la fin 2020 (sous réserve du succès des travaux précliniques et de l'obtention de financements) o Production des lots cliniques prévue sur le site de Valneva situé à Livingston, Ecosse, qui est approuvé par la FDA
David Lawrence, Directeur financier de Valneva, a indiqué, “Compte tenu de la pandémie actuelle, nous sommes très satisfaits de nos résultats financiers du premier trimestre. Nous avons également conclu un accord de collaboration sans précédent avec Pfizer pour faire avancer notre programme contre la maladie de Lyme en réponse à un besoin médical majeur non satisfait. Compte tenu de la crise mondiale du COVID-19 et de son impact significatif sur notre activité de vaccins du voyage, nous nous réjouissons de pouvoir équilibrer le bien-être de nos employés et la continuité de nos activités, et nous tenons à les remercier pour leur engagement et leur flexibilité".
========================================
Saint Herblain (France), 7 mai 2020 – Valneva SE (“Valneva” ou “le Groupe”), société spécialisée dans les vaccins contre les maladies générant d’importants besoins médicaux, publie aujourd’hui ses résultats financiers du premier trimestre clos au 31 mars 2020. Les résultats financiers intermédiaires consolidés sont disponibles sur le site internet de la société www.valneva.com. Valneva retransmettra en direct la conférence téléphonique sur les résultats financiers du premier trimestre à 15h00 CEST sur le site internet du Groupe via le lien : https://edge.media- server.com/mmc/p/5i6xunqx
Vaccins commerciaux
• VACCIN CONTRE L’ENCEPHALITE JAPONAISE (IXIARO®/JESPECT®)
Au premier trimestre 2020, les ventes du vaccin IXIARO®/JESPECT® ont atteint €22,9 millions, soit une croissance de 2% (0% à taux de change constant). Cette augmentation a été principalement soutenue par la demande de produits en Amérique du Nord, sur les marchés public et privé. Au cours du premier trimestre 2020, le département américain de la défense (“DoD”) a publié un appel d’offres (RFP) pour la fourniture de vaccins contre l’encéphalite japonaise à l’armée américaine. En tant que fournisseur du seul vaccin contre l’encéphalite japonaise approuvé par l’agence de santé américaine FDA, Valneva a répondu à cet appel d’offres et prévoit de signer un nouveau contrat avec le DoD au second trimestre de cette année. Ce nouveau contrat devrait être le principal moteur des ventes d’IXIARO®/JESPECT® en 2020 et au-delà. La FDA a, par ailleurs, approuvé en mars 2020 une prolongation de la durée d’utilisation du vaccin contre l’encéphalite japonaise IXIARO® de 24 à 36 mois6, facilitant ainsi la gestion de l’approvisionnement du vaccin.
• VACCIN CONTRE LE CHOLERA / LA DIARRHEE LIEE A L’ETEC 7 (DUKORAL®)
Au premier trimestre 2020, les ventes de DUKORAL® ont progressé à €9,7 millions contre €9.6 millions au premier trimestre 2019.
• MARCHÉ DES VACCINS DU VOYAGE
Le groupe prévoit que les vaccins IXIARO®/JESPECT® et DUKORAL® vont être significativement impactés par le ralentissement du marché du voyage, notamment au deuxième et troisième trimestres 2020, avec une reprise progressive du marché anticipée au quatrième trimestre. Bien que cela puisse prendre des années pour que le marché du voyage revienne à ses niveaux précédents, le Groupe pense que la crise actuelle pourrait avoir un impact positif sur le marché du vaccin à moyen et long terme en raison d’une sensibilisation accrue à la vaccination.
Candidats vaccins en développement clinique
• CANDIDAT VACCIN CONTRE LA MALADIE DE LYME – VLA15
Alliance stratégique avec Pfizer; Premiers résultats de Phase 2 attendus mi 2020 Le vaccin contre la maladie de Lyme de Valneva, VLA15, est actuellement le seul programme clinique actif au monde à cibler la maladie transmise par les tiques la plus commune de l’hémisphère nord. Valneva a récemment annoncé la signature d’un accord de partenariat majeur avec Pfizer pour le développement avancé et la future commercialisation de VLA158. Valneva et Pfizer travailleront en étroite collaboration pendant tout le développement de VLA15. Valneva pourra recevoir des paiements d’un montant total de $308 millions dont un paiement initial de $130 millions, des paiements d’étape de $35 millions liés à l’avancée du développement du produit et jusqu’à $143 millions de paiements additionnels liés aux premières étapes de commercialisation du produit.
Selon les termes de l’accord, Valneva financera 30% de tous les coûts de développement jusqu’à la fin du programme de développement et en retour, Pfizer versera à Valneva des redevances croissantes sur les ventes, avec un taux débutant à 19%. Pfizer dirigera les activités liées aux dernières étapes de développement du vaccin et sera seul en charge de la commercialisation. Valneva a finalisé le recrutement et le suivi de plus de 800 patients dans les deux études de Phase 2 de son vaccin contre la maladie de Lyme.
Le Groupe prévoit de publier les premiers résultats de l’étude VLA15-201 pour le schéma de vaccination le plus court (Jour 1, Mois 1 et Mois 2) en juillet 2020 suivi, au troisième trimestre, par les premiers résultats de l’étude VLA15-202 (Jour 1, Mois 2 et Mois 6). Les résultats des études de Phase 2 vont permettre, sur la base des données d’immunogénicité et d’innocuité, d’identifier le dosage et le schéma de vaccination à utiliser pour la Phase 3.
Selon les organismes américains de contrôle et de prévention des maladies (CDC), environ 300 000 américains9 sont diagnostiqués chaque année et au moins 200 000 cas seraient également recensés chaque année en Europe10. VLA15 est un vaccin multivalent à sous-unités de protéines ciblant la surface externe de la protéine A (OspA) de la Borrelia dont l’objectif est d’offrir une protection contre la majorité des souches de Borrelia pathogènes.
VLA15 est conçu pour offrir une protection contre la maladie de Lyme en augmentant le niveau des anticorps qui empêchent la bactérie Borrelia de migrer de la tique à l’homme après une morsure. Le programme a reçu le statut de “Fast track” de l’autorité de santé américaine, FDA, en juillet 201711
. Le potentiel de chiffre d’affaires pour un vaccin contre la maladie de Lyme, Etats-Unis et Europe conjugués, est estimé à plus de $1 milliard12.
• CANDIDAT VACCIN A INJECTION UNIQUE CONTRE LE CHIKUNGUNYA – VLA1553
Préparation pour l’initiation de la Phase 3 actuellement en cours Le candidat vaccin de Valneva à injection unique contre le chikungunya, VLA1553, cible une infection transmise par les moustiques et fortement prévalente dans les régions tropicales et subtropicales. Valneva prévoit de développer ce produit jusqu’à sa mise sur le marché avec l’intention d’en retirer des synergies industrielles et commerciales extrêmement importantes en se concentrant dans un premier temps sur le marché du voyage. Valneva et l’Institut brésilien Butantan ont récemment annoncé la signature d’une lettre d’intention liante (binding term sheet) pour le développement, la production et la commercialisation du candidat vaccin à dose unique de Valneva contre le chikungunya, VLA1553, dans les pays à revenus faibles et intermédiaires13.
Cette collaboration s’inscrit dans le cadre du financement de $23,4 millions que Valneva a reçu de la Coalition pour les Innovations en Préparation aux Epidémies (CEPI) en juillet 201914.
Au cours du premier trimestre 2020, Valneva a tenu une réunion de fin de Phase 2 avec l’agence de santé américaine (FDA)15. Valneva continue à advancer sur la preparation de la Phase 3, y compris avec son organisme de recherche sous contrat (CRO) afin de pouvoir initier la Phase 3 dès que la situation liée au COVID-19 le permettra. Comme précédemment annoncé, le Groupe prévoit d’initier les essais cliniques de Phase 3 au quatrième trimestre de cette année, soit trois mois plus tard que prévu initialement.
Le chikungunya est considéré comme une menace majeure pour la santé publique, et aucun vaccin préventif ou traitement efficace n’est actuellement disponible. Le virus chikungunya (CHIKV) est un alphavirus de la famille des Togaviridae transmis par les moustiques Aedes. Depuis 2017, plus d’un million de cas ont été recensés sur le continent américain16 et l’impact économique de la maladie est considéré comme extrêmement important (ex. l’épidémie de la Colombie en 2014 : $73,6 million17). Cet impact devrait continuer à s’alourdir alors que les principaux vecteurs du virus ne cessent d’étendre leur territoire. VLA1553 est un candidat vaccin monovalent vivant atténué visant à offrir une protection contre le virus chikungunya. Il a reçu le statut de « Fast Track » de la FDA en décembre 2018.
Le marché mondial total des vaccins contre le chikungunya vaccines est estimé à plus de $500 millions19 et le marché du voyage à environ $250 millions.
La société dont le vaccin contre le chikugununya recevra la première autorisation de mise sur le marché aux Etats-Unis sera éligible à l’obtention d’un bon d’évaluation prioritaire (Priority Review Voucher).
• CANDIDAT VACCIN contre le virus SARS-COV-2 – VLA 2001
Programme de développement d’un vaccin inactivé récemment initié
Valneva a récemment initié un programme de recherche visant à développer un vaccin contre le virus SARS-CoV-2, l’agent pathogène du COVID-1921. Le Groupe s’appuie sur la plateforme précédemment approuvée pour son vaccin IXIARO® afin de développer un candidat vaccin inactivé et adjuvanté en collaboration avec Dynavax.
Dynavax fournit son adjuvant CpG 1018, qui est par ailleurs incorporé dans HEPLISAV-B®, un vaccin contre l’hépatite B approuvé par la FDA (U.S. Food and Drug Administration). Valneva mène des travaux de développement préclinique dans ses laboratoires de niveau 3 de biosécurité et a alloué au projet des ressources provenant de ses autres projets en tout début de développement (recherche initiale et développement pré-clinique), sans affecter le développement clinique de ses candidats vaccins contre la maladie de Lyme et le chikungunya. Valneva et Dynavax vont travailler de concert avec les autorités réglementaires pour s’accorder sur la stratégie optimale pour un développement clinique accéléré, avec pour objectif d’initier des essais cliniques avant la fin 2020 (sous réserve de la réussite des travaux précliniques et de l'obtention d'un financement approprié).
Valneva possède les compétences nécessaires à la production de ce type de vaccin viral dans son usine de Livingston (UK), opérant selon les normes BPF, et prévoit de produire les lots cliniques dans cette usine.
Valneva recherche des financements non dilutifs, et notamment des subventions, pour le développement clinique et les investissements industriels nécessaires. Si le programme est un succès et obtient les financements appropriés, Valneva estime que sa capacité de production initiale pourrait dépasser les 30 millions de doses par an.
=======================================
Eléments financiers du premier trimestre 2020 (non-audités, consolidés selon les normes IFRS)
Chiffre d’affaires
Le chiffre d’affaires total de Valneva était de €35,2 millions au premier trimestre de l’exercice 2020, contre €34,9 millions au premier trimestre de l’exercice 2019. Les ventes de produits se sont élevées à €32,7 millions au premier trimestre 2020 contre €32,8 millions sur la même période en 2019. A taux de change constants, les ventes de produits ont diminué de 2% par rapport au premier trimestre 2019. Le chiffre d’affaires des collaborations et licences était de €2,5 millions au premier trimestre 2020 contre €2,1 millions sur la même période en 2019.
Résultat opérationnel et EBITDA
Les coûts des produits et services vendus (COGS) étaient de €12,1 millions au premier trimestre de l’exercice 2020, soit une marge brute totale de 69,4% contre 66,3% au premier trimestre 2019. €6,7 millions de ces coûts provenaient des ventes d’IXIARO®/JESPECT®, soit une marge brute de 70,8% pour ce vaccin, et €3,2 millions de ces coûts provenaient des ventes de DUKORAL®, soit une marge brute de 66,8% pour ce vaccin. Sur les coûts restants au premier trimestre 2020, €0,1 million provenait de l’activité de distribution de produits pour tiers et €2,1 millions des coûts des services. Au premier trimestre de l’exercice 2019, les COGS étaient de €12,2 millions, dont €11,1 millions liés aux coûts des produits et €1,1 million lié aux coûts des services.
Les dépenses de Recherche et développement (R&D) étaient de €13,3 millions au premier trimestre 2020 contre €6,3 millions sur la période de comparaison en 2019. Cette progression attendue est liée à une augmentation des investissements dans les candidats vaccins en développement clinique de Valneva. Au premier trimestre 2020, les frais commerciaux étaient de €6,0 millions contre €5,6 millions au premier trimestre 2019. Les frais généraux et administratifs ont, quant à eux, progressé de €5,2 millions au premier trimestre 2020 contre €4,5 millions sur la même période de l’exercice 2019, principalement en raison d’une augmentation des coûts destinés à soutenir les projets stratégiques du Groupe et de la mise en place d’un nouveau programme de souscriptions d’actions pour les employés du Groupe. Les charges d’amortissement et de dépréciation d’actifs sont demeurées inchangées par rapport à la même période de 2019 et étaient de €0,7 million au premier trimestre 2020.
Les autres revenus, nets des autres charges, ont progressé à €2,2 millions au premier trimestre 2020 contre €0,8 millions au premier trimestre 2019. Cette hausse s’explique par l'augmentation du crédit d'impôt Recherche et des revenus provenant du financement CEPI pour le programme chikungunya de Valneva.
Valneva a réalisé un bénéfice opérationnel de €0,1 million au premier trimestre 2020 contre un bénéfice opérationnel de €6,2 millions sur la même période en 2019. Le Groupe a, par ailleurs, enregistré un EBITDA de €2,4millions au premier trimestre 2020 contre un EBITDA de €8,2 millions au premier trimestre 2019.
Résultat net
Au premier trimestre de l’exercice 2020, Valneva a généré une perte nette de €1,2 million contre un bénéfice net de €4,9 millions au premier trimestre 2019. Les charges financières et effets de change au premier trimestre 2020 ont résulté en un résultat financier négatif de €2,2 millions comparé à un résultat financier positif de €0,5 millions au premier trimestre de l’exercice 2019. Ce recul s’explique par une augmentation des intérêts débiteurs et des pertes de change principalement du fait de la nouvelle dette contractée en dollars
Flux de trésorerie et liquidités
Les flux nets de trésorerie générés par les activités opérationnelles se sont élevés à €3,0 millions au premier trimestre 2020 contre €5,3 millions au premier trimestre 2019.
Les flux de trésorerie négatifs liés aux activités d’investissement étaient de €0,6 million au premier trimestre 2020, contre €0,8 million au premier trimestre 2019.
Les flux de trésorerie positifs liés aux activités de financement étaient de €14,5 millions au premier trimestre 2020 et comprenaient €35,5 millions de produits nets provenant de l’accord de financement signés avec les fonds américains spécialistes du secteur de la santé Deerfield & Orbimed ainsi que €20,0 millions de remboursement d’emprunt auprès de la Banque Européenne d’Investissement (BEI). Les flux de trésorerie négatifs liés aux activités de financement étaient de €13,5 millions au premier trimestre 2019 dont le remboursement du prêt Biopharma (Pharaon).
La trésorerie du Groupe au 31 mars 2020 était de €80,8 millions contre €64,4 millions au 31 décembre 2019. Cette variation résulte principalement du produit de la nouvelle dette auquel a été soustrait le montant de l’emprunt remboursé à la BEI.
A propos de Valneva SE
Valneva est une société spécialisée dans les vaccins contre les maladies générant d’importants besoins médicaux. Le portefeuille de produits de Valneva inclut deux vaccins du voyageur, IXIARO®/JESPECT® contre l’encéphalite japonaise et DUKORAL®22 dans la prévention du choléra et, dans certains pays, de la diarrhée causée par l’ETEC. Le groupe est également propriétaire d’un solide portefeuille de vaccins en développement dont le seul candidat vaccin en phase clinique contre la maladie de Lyme. Valneva compte plus de 500 employés et exerce ses activités depuis l’Autriche, la Suède, la Grande-Bretagne, la France, le Canada et les Etats-Unis. Pour plus d’information, consulter le site internet du Groupe www.valneva.com et suivez la société sur LinkedIn.
|
Répondre
|
ça consolide sur 4 euros.Je me place.
|
Répondre
|
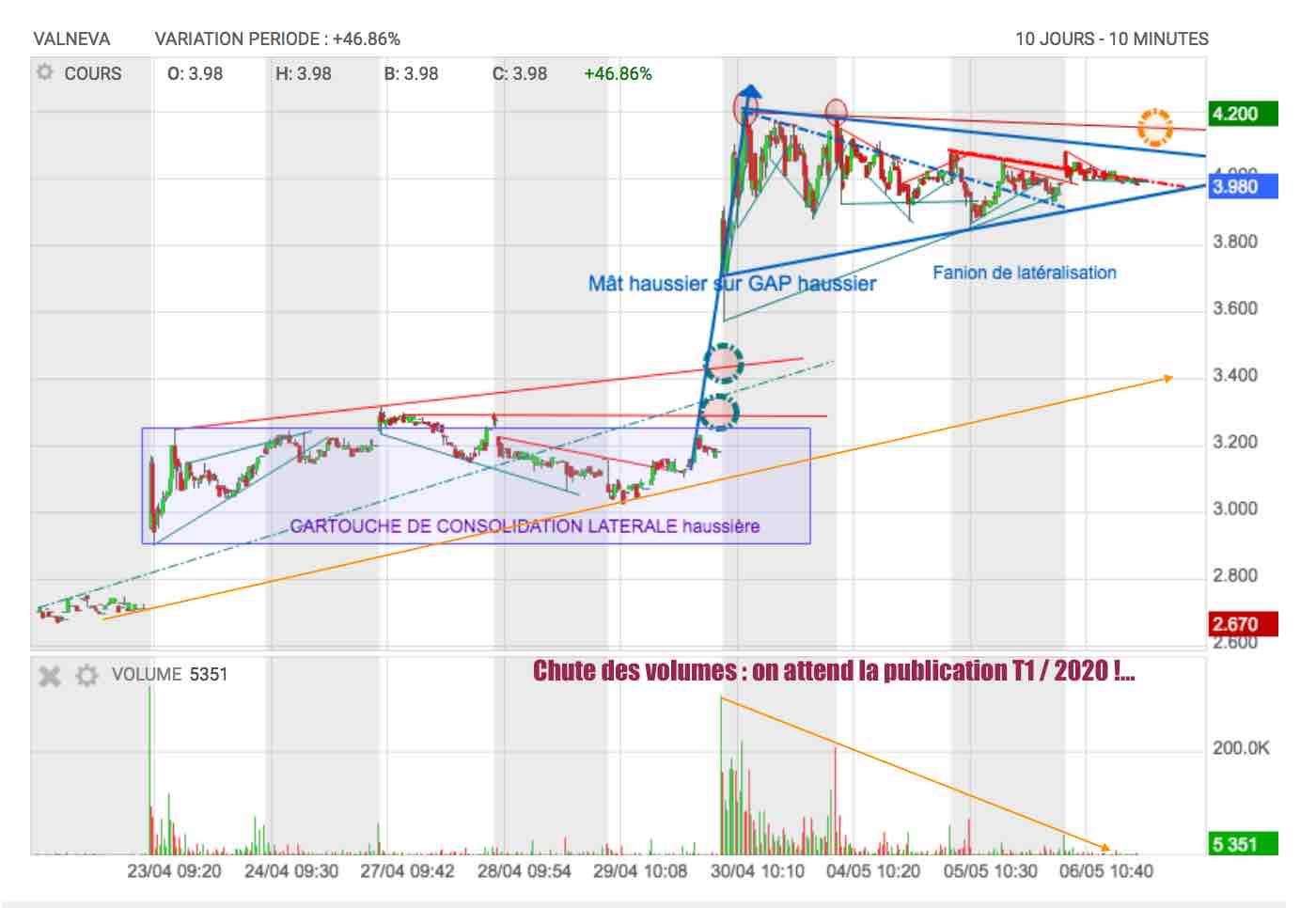
La pression haussière monte d'un cran ...
Y'en a plus de volume en intraday et on a tout exploité le fanion, c'est tout près pour demain...
: )
Graphe indraday sur 10 jours : Le drapeau haussier s'est fait sur une annonce d'un versement de 130 Millions, c'est bien mieux qu'une augmentation de capital et c'est le N°1 sur le marché des vaccins qui investit dans les projets de Valneva.
A suivre vraiment !
.
Message complété le 06/05/2020 14:59:24 par son auteur.
Vous noterez que l'on perdu toute amplitude graphique aujourdhui : c'est donc qu'il va se passer quelque chose ...
.
|
Répondre
|
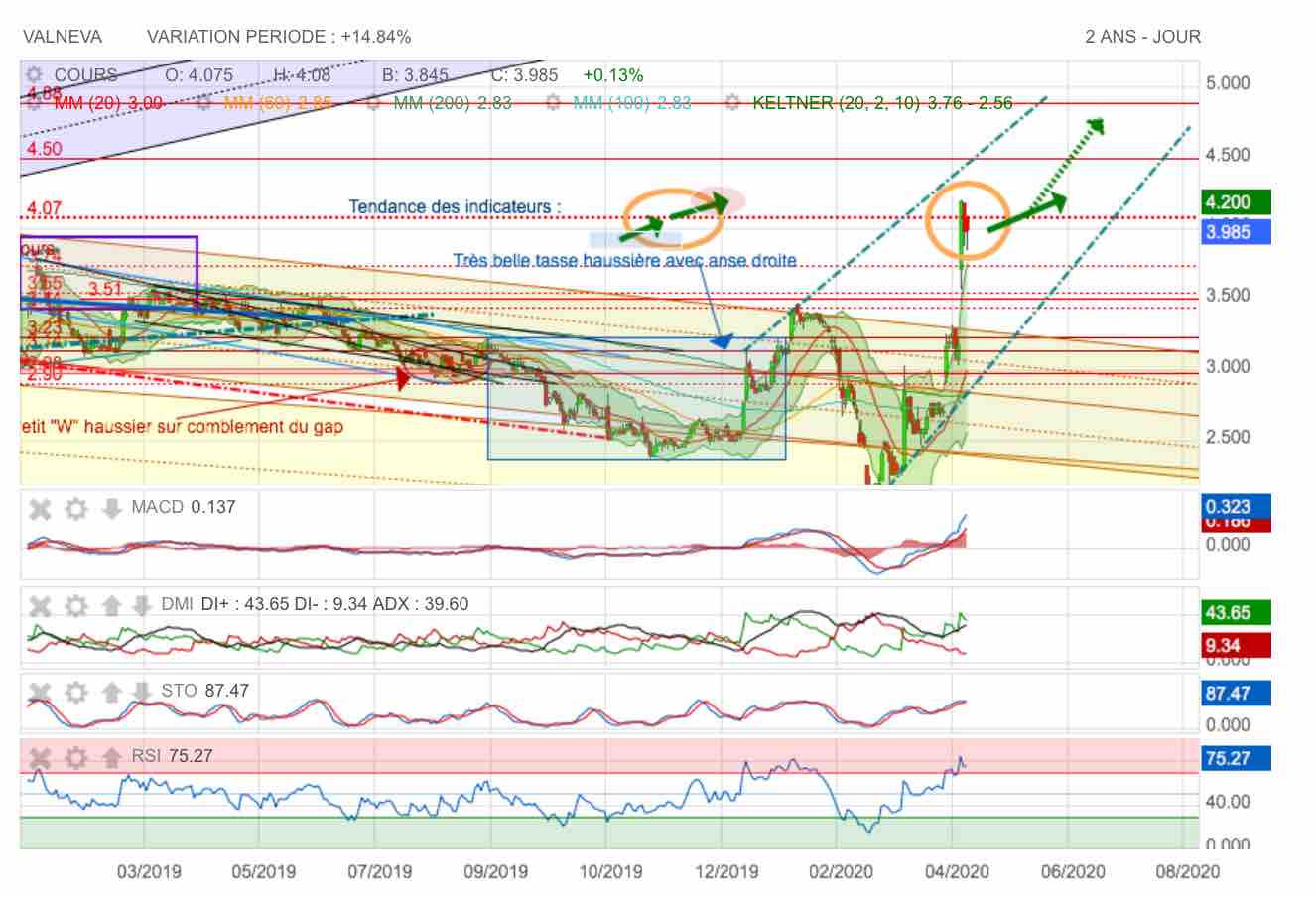
Les indicateurs haussiers à bloc à J-2 de la publication trimestrielle...
Et vu ce qui a été annoncé, ça devrait rassurer nettement ... On devrait une bonne livrée concernant les projets en cours.
Pression très nette de surachat sur le RSI : le MACD se cabre littéralement...
.
|
Répondre
|
VALNEVA : PORTZAMPARC À 5.1 €
30 avril 2020
"Cet accord qui survient après le désistement de GSK est une très belle revanche pour le produit phare de la société" commente Portzamparc. "Le fait que Pfizer se positionne avant même l'annonce des résultats de phase 2 témoigne également de sa très grande confiance quant au potentiel du produit... Sur le plan financier, l'upfront permettra de couvrir largement le financement du programme (phase 3 évaluée à environ 350 M$ dont 30% à la charge de Valneva), mais également les autres programmes prioritaires dont l'étude de phase 3 dans le Chikungunya qui débutera cette année.
En outre nous estimons que le 'deal' dé-risque significativement le modèle économique de Valneva" poursuit l'analyste qui conclut : "Après prise en compte des modalités financières du deal, nous relevons notre TP de 3,2 à 5,1 euros".
|
Répondre
|
 Suivez les marchés avec des outils de pros !
Suivez les marchés avec des outils de pros !