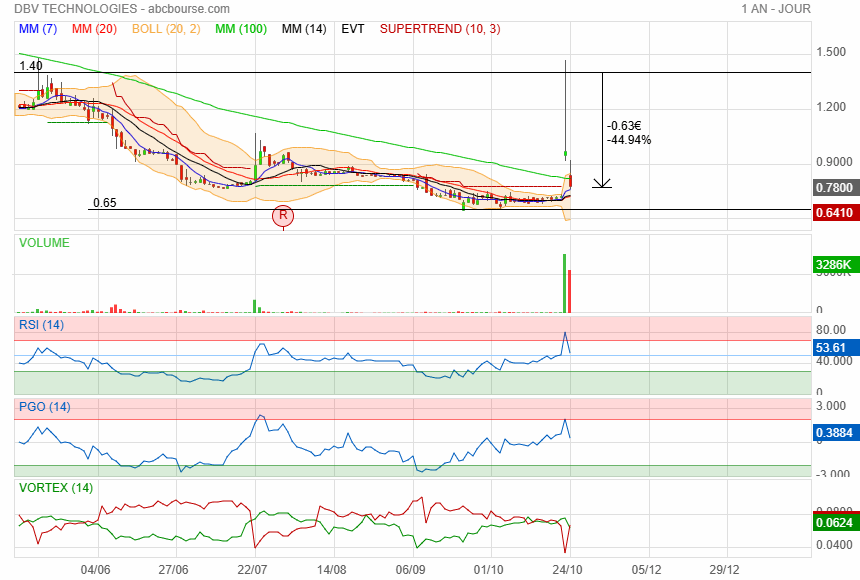
L'admission au SBF120 et la publication des résultats semblent plutôt bien appréciés
Message complété le 27/03/2026 11:56:06 par son auteur.
*appréciées
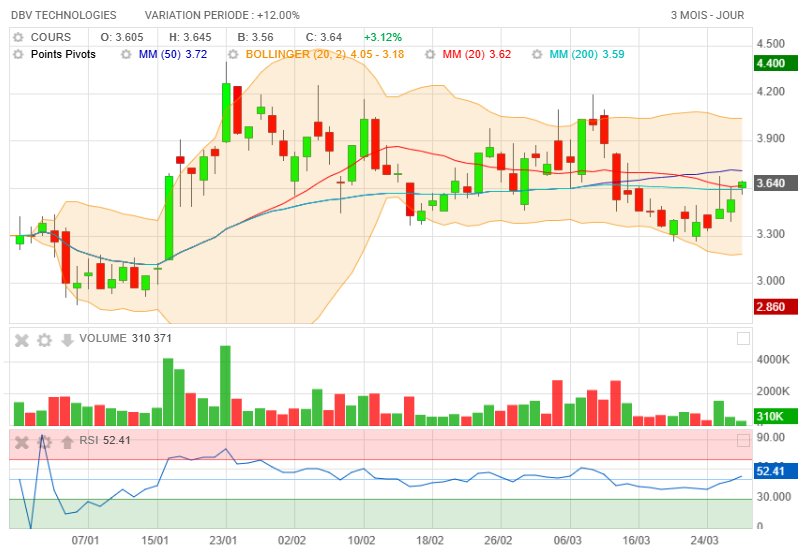
DBV technologies confirme sa visibilite financiere jusqu’au deuxieme trimestre 2027
Avec une annonce pareille elle devrait etre a 5!!Sans doute que tout n’a pas été dit....un broker l’annknce bien plus haute et elle baisse.
Cela fait 5 ans que cette action est à la ramasse........doit on vraiment y croire après les propos de ce jour du DG.
Quelle est l annonce qui l a fait monter? Peut on viser 4 ou 5 ou bien un cadeau de noel cette hausse!!!
Quelle est l annonce qui l a fait monter? Peut on viser 4 ou 5 ou bien un cadeau de noel cette hausse!!!
Ça fait quelques années que j'attends la bonne nouvelle. Mais lesquelle ?
C'est facile a dire mais pas évident a faire
même scotché sur ce genre de boite faut avoir le courage de vendre quand il y a explosion et éventuellement revenir sur le titre au plus bas par la suite
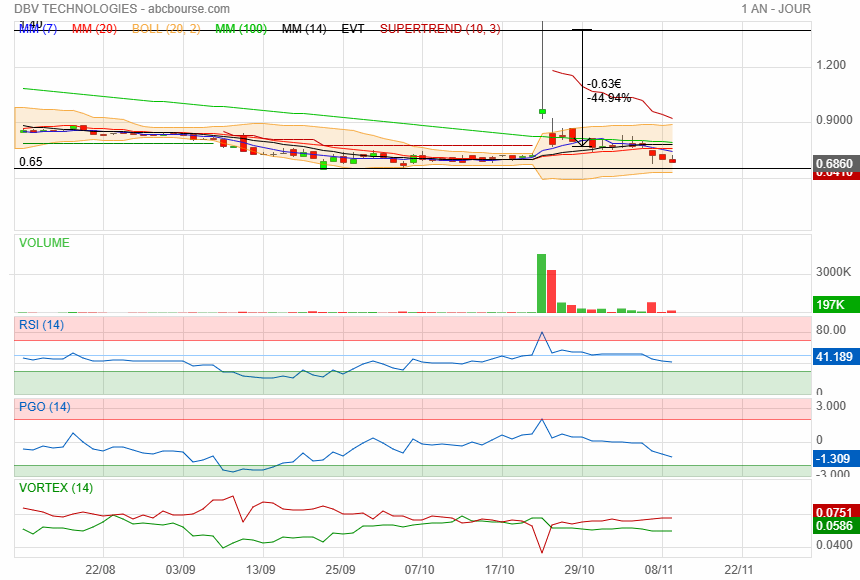
Et voila un plus bas, société de merde comme toutes ces entreprises francaises mal gouverné ou les dirigeants s'octroies des salaires de dingues !!!
C'est bien ce que je craignais........une société de merde avec des dirigeants de merde qui j'en suis certain se donnent des salaires de prince comme la plupart des biotechs françaises
Bonjour Twarog, le père Noêl c'est pour les enfants.......pas pour la bourse. Désolé pour toi et moi.
+10% !
Je attends depuis 3 ans je peux attendre encore 3 mois ! Si en janvier FDA accepte pour l’enfant 1-3 ans peut être je vais retrouver mon PRU 😮💨🥴👋
« Notre accord avec la FDA sur une procédure accélérée pour le patch Viaskin Peanut chez enfants âgés de 1 à 3 ans représente une étape importante dans la mise à disposition de ce nouveau traitement pour les patients », a déclaré Daniel Tassé, Directeur Général de DBV Technologies. « Je suis heureux que la FDA reconnaisse le besoin médical urgent non satisfait qui existe pour cette jeune population de patients. Nous sommes également très satisfaits de l’avis scientifique reçu de l’EMA, à savoir un patch unique pour les enfants allergiques à l’arachide âgés de 1 à 7 ans, dès lors que l’étude d’innocuité avec le patch modifié chez les 1 à 3 ans aura été réalisée ».
Patch Viaskin Peanut chez les enfants de 1 à 3 ans
Procédure d’approbation accélérée
Les directives de la FDA relatives à l’approbation accélérée comprennent trois critères de qualification : 1) le produit doit traiter une maladie grave, 2) le produit doit apporter un avantage significatif par rapport aux thérapies disponibles, et 3) le produit doit démontrer un effet sur un critère clinique intermédiaire, raisonnablement susceptible de prédire un bénéfice clinique.
La FDA a confirmé que DBV a déjà satisfait aux critères 1 et 2. En ce qui concerne le critère 3, la FDA a fourni des orientations et des suggestions concernant le critère clinique intermédiaire, que DBV a accepté lors de discussions informelles avec la FDA. DBV prévoit de formaliser ces directives en sollicitant une réunion formelle pour confirmer les composantes générales des deux études concernées : l’étude d’innocuité COMFORT Toddlers, qui doit être achevée avant le dépôt du BLA, ainsi que l’étude de confirmation d’efficacité, y compris le troisième critère d’approbation accélérée relatif au critère clinique intermédiaire. DBV prévoit que l’étude de confirmation soit lancée au moment du dépôt du BLA, et se déroule parallèlement à la commercialisation aux États-Unis, si Viaskin Peanut est approuvé.
Je attends depuis 3 ans je peux attendre encore 3 mois ! Si en janvier FDA accepte pour l’enfant 1-3 ans peut être je vais retrouver mon PRU 😮💨🥴👋
« Notre accord avec la FDA sur une procédure accélérée pour le patch Viaskin Peanut chez enfants âgés de 1 à 3 ans représente une étape importante dans la mise à disposition de ce nouveau traitement pour les patients », a déclaré Daniel Tassé, Directeur Général de DBV Technologies. « Je suis heureux que la FDA reconnaisse le besoin médical urgent non satisfait qui existe pour cette jeune population de patients. Nous sommes également très satisfaits de l’avis scientifique reçu de l’EMA, à savoir un patch unique pour les enfants allergiques à l’arachide âgés de 1 à 7 ans, dès lors que l’étude d’innocuité avec le patch modifié chez les 1 à 3 ans aura été réalisée ».
Patch Viaskin Peanut chez les enfants de 1 à 3 ans
Procédure d’approbation accélérée
Les directives de la FDA relatives à l’approbation accélérée comprennent trois critères de qualification : 1) le produit doit traiter une maladie grave, 2) le produit doit apporter un avantage significatif par rapport aux thérapies disponibles, et 3) le produit doit démontrer un effet sur un critère clinique intermédiaire, raisonnablement susceptible de prédire un bénéfice clinique.
La FDA a confirmé que DBV a déjà satisfait aux critères 1 et 2. En ce qui concerne le critère 3, la FDA a fourni des orientations et des suggestions concernant le critère clinique intermédiaire, que DBV a accepté lors de discussions informelles avec la FDA. DBV prévoit de formaliser ces directives en sollicitant une réunion formelle pour confirmer les composantes générales des deux études concernées : l’étude d’innocuité COMFORT Toddlers, qui doit être achevée avant le dépôt du BLA, ainsi que l’étude de confirmation d’efficacité, y compris le troisième critère d’approbation accélérée relatif au critère clinique intermédiaire. DBV prévoit que l’étude de confirmation soit lancée au moment du dépôt du BLA, et se déroule parallèlement à la commercialisation aux États-Unis, si Viaskin Peanut est approuvé.
Eh oui, tout le monde s'est jeté dessus, et aujourd'hui patatra........c'est DBV ........une merde.
Moi je suis bloqué avec PRU énorme ! Seulement D’accord FDA va me libérer… 🥴😤👋
Forum de discussion Dbv Technologies
202603271103 1049547