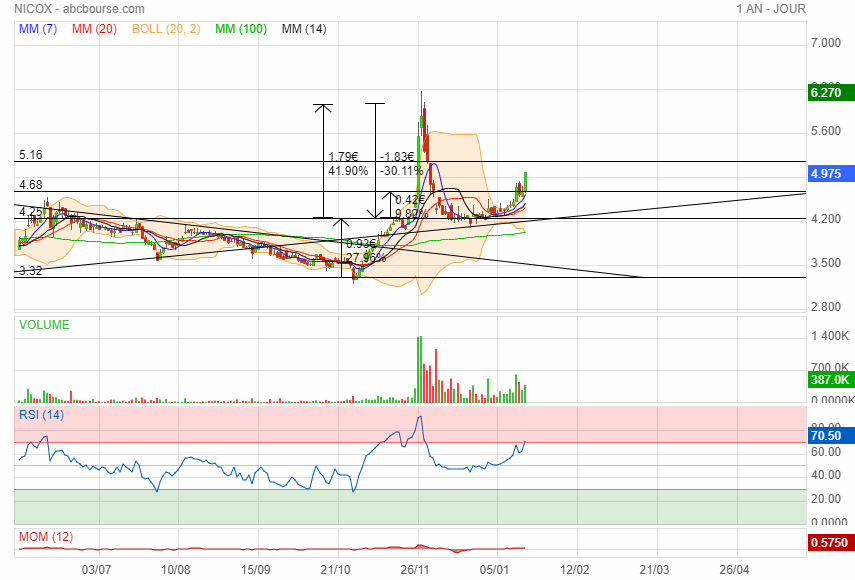
Bryan Garnier coupe son objectif sur Nicox de 17,5 à 11 euros mais reste à l''achat'.
17 novembre 2021 :
Nicox : Délivrance d’un brevet européen pour le NCX 4251, candidat médicament en développement pour la blépharite
Message complété le 17/11/2021 09:07:21 par son auteur.
Nicox annonce aujourd'hui la délivrance par l'Office Européen des Brevets (OEB) du brevet EP 3,769,753 qui couvre jusqu'en 2040 le NCX 4251, candidat médicament en développement pour la blépharite.
Ce brevet couvre les suspensions ophtalmiques comprenant une forme spécifique de nanocristaux de propionate de fluticasone ainsi que le procédé de fabrication des suspensions ophtalmiques. Des demandes de brevet ayant le même objet sont en cours d'examen aux États-Unis, en Chine, au Japon et dans d'autres territoires.
+55% depuis mon post du 29/10/2020 à 08:51:53
Message complété le 26/11/2020 14:13:16 par son auteur.
+70% depuis mon post du 29/10/2020 à 08:51:53
Oui, la rumba c’est fondamental. Merci pour ton analyse Pif Poche 😊
Boursier 29/10/2020 07:33 Nicox : nouveau brevet délivré pour le NCX 470, exclusivité prolongée en Europe jusqu'en 2039
Nicox annonce qu'un brevet de formulation couvrant le NCX 470 a été délivré par l'Office Européen des Brevets, prolongeant l'exclusivité européenne de...
Nicox annonce qu'un brevet de formulation couvrant le NCX 470 a été délivré par l'Office Européen des Brevets, prolongeant l'exclusivité européenne de la protection du NCX 470 jusqu'en 2039. Un brevet équivalent a déjà été délivré aux Etats-Unis et le NCX 470 est également protégé par un brevet couvrant sa composition de matière.
Gavin Spencer, Chief Business Officer de Nicox, a déclaré : "Nous sommes très satisfaits de la délivrance de ce brevet de formulation pour le NCX 470 en Europe, suite à celle d'un brevet américain plus tôt cette année. Ceci renforce notre position en fournissant une protection supplémentaire à ce candidat médicament, potentiellement meilleur de sa classe, qui est actuellement en développement clinique de phase 3 en vue d'une future commercialisation pour la réduction de la pression intraoculaire."
-----------------------------------------
*: Actionnaire
Message complété le 29/10/2020 09:29:04 par son auteur.
Timide la Nicox, Cours temps réel: 3,365€ 2,59%
Érection proche?
26/10/2020 08:53 NICOX : feu vert de la Chine à l'étude de phase 3 sur le NCX 470 pour la PIO
*:Actionnaire pas une incitation.....
Je t'aime aussi !
Grrr ! 😡
Message complété le 23/10/2020 11:34:30 par son auteur.
@ Ribo 🤭
Salut JD, t'as trouvé une nouvelle Vallourec ?
23/10/2020 08:53 | AOF
NICOX étend son portefeuille avec un troisième programme novateur Credits ShutterStock.com
Nicox a sélectionné un nouveau candidat au développement, le NCX 1728, issu de son programme de recherche de composés brevetés axé sur des composés modulés par l'oxyde nitrique (NO) réduisant la pression intraoculaire (PIO). Un analogue de cette molécule a démontré1 des résultats positifs chez des primates non humains présentant une hypertension oculaire en comparaison avec le travoprost 0,1%, un analogue de prostaglandine. Les analogues de prostaglandines sont le traitement standard pour la réduction de la PIO.
Nicox détient les droits exclusifs mondiaux du NCX 1728. Une optimisation complémentaire des formulations ophtalmiques sera effectuée avant d'initier les tests formels préalables nécessaires au dépôt d'un dossier d'Investigational New Drug (IND).
NICOX : point sur l’avancement de l'étude clinique Mont Blanc dans le glaucome
15/07/2020 08:32
Nicox SA a annoncé que plus de 40 sites cliniques sont opérationnels, et ce dès lepremier mois de l'étude de phase 3 Mont Blanc qui vise à évaluer le NCX 470 pour la réduction de la pression intraoculaire (PIO) chez des patients atteints de glaucome à angle ouvert ou d'hypertension oculaire. NCX 470 est le nouvel analogue de bimatoprost donneur d'oxyde nitrique (NO) de deuxième génération de Nicox.
L'étude Mont Blanc est une étude internationale, en double insu, d'une durée de 3 mois, en groupes parallèles, avec un design adaptatif visant à évaluer l'efficacité et la sécurité de la solution ophtalmique de NCX 470 à 0,065% et à 0,1% par rapport à la solution ophtalmique de latanoprost à 0,005% chez des patients atteints de glaucome à angle ouvert ou d'hypertension oculaire.
“Suite aux résultats prometteurs de notre étude de phase 2 Dolomites, NCX 470 a le potentiel d'apporter une amélioration par rapport à la thérapie de référence actuelle pour les patients avec une PIO élevée. La sélection du dosage de NCX 470 dans la partie adaptative de l'étude devrait être finalisée d'ici la fin de l'année 2020, permettant ainsi de mener le reste de l'étude Mont Blanc et de démarrer notre seconde étude de phase 3 Denali en 2020 ” a déclaré Tomas Navratil, PhD, EVP, Head of R&D du groupe Nicox et General Manager de Nicox Ophthalmics, Inc.
31/03/2020 | 07:30►Nicox : Lancement de ZERVIATETM aux Etats-Unis par son partenaire Eyevance Pharmaceuticals
ZERVIATE nouvelle source de revenu récurrente avec ce deuxième produit de Nicox licencié et commercialisé aux Etats-Unis
ZERVIATE commercialisé par Eyevance, une société émergente spécialisée en ophtalmologie axée sur les traitements de la surface oculaire et du segment antérieur de l’oeil
https://ml-eu.globenewswire.com/Resource/Download/83108463-217d-450c-b85f-80e8775106b4
06/03/2020 ►Nicox : Résultats financiers 2019 et étapes clé en 2020.
19/03/2019 | 07:30 Nicox : Initiation d'une étude de phase 2 pour le NCX 4251 dans la blépharite
Communiqué de presse
Nicox : Initiation d'une étude de phase 2 pour le NCX 4251 dans la blépharite
................................................
Etude randomisée sur 30 patients répartis dans des sites cliniques aux Etats-Unis
Premiers résultats attendus au quatrième trimestre 2019
Vise le marché de la blépharite aux Etats-Unis d'un montant estimé à plus de 500 millions de dollars
.................................................
19 mars 2019 - diffusion à 7h30 Sophia Antipolis, France
Nicox SA (Euronext Paris: FR0013018124, COX, éligible PEA-PME), une société internationale spécialisée en ophtalmologie, annonce l'initiation d'une étude clinique de phase 2 afin d'évaluer le NCX 4251, sa nouvelle suspension brevetée de nanocristaux de propionate de fluticasone, développé comme premier traitement topique ciblé du bord de la paupière chez les patients présentant des épisodes aigus de blépharite. Nicox prévoit de communiquer les premiers résultats de cette étude de phase 2 au cours du quatrième trimestre 2019.
Cette étude de phase 2 multicentrique, randomisée, menée en double aveugle, versus placebo, en dose croissante, d'une durée de 14 jours a pour objectif d'évaluer la sécurité et la tolérabilité du NCX 4251 par rapport au placébo chez des patients présentant des épisodes aigus de blépharite. Environ 30 patients répartis dans des sites cliniques aux Etats-Unis devraient être randomisés au cours de l'étude. L'objectif principal de cette étude clinique est la sélection de la/ des dose(s) appropriée(s) de NCX 4251 pour passer à l'étape suivante de développement qui sera une étude clinique plus large de phase 2b.
Tomas Navratil, PhD, Executive Vice President, Head of Development de Nicox, a déclaré : "Il n'y a pas de produit approuvé aux Etats-Unis uniquement pour le traitement de la blépharite. Nous pensons qu'un produit efficace et mieux toléré pour le traitement de la blépharite pourrait résulter de la combinaison d'un puissant corticostéroïde dans notre nouvelle suspension nanocrystalline avec une application directement à l'endroit de l'inflammation, foyer de la pathologie."
Michele Garufi, Président directeur général de Nicox a commenté : "Pour la Société, le démarrage de ce second programme clinique, après l'initiation de l'étude clinique du NCX 470 pour la réduction de la pression intraoculaire en août l'an dernier, représente une grande réalisation pour notre équipe de développement. Avec deux produits commerciaux, deux candidats médicaments à un stade intermédiaire de développement clinique et deux programmes de recherche innovants, nous poursuivons la construction d'une société unique et pleinement intégrée dans le domaine de l'ophtalmologie."
L'initiation de cette étude de phase 2 fait suite à l'aval de la Food and Drug Administration (FDA) américaine pour le dossier d'Investigational New Drug (IND) soumis en décembre 2018, soit avant la date prévue au premier trimestre 2019.
A propos de NCX 4251
NCX 4251 est une suspension novatrice, brevetée, de nanocristaux de propionate de fluticasone qui est développée comme premier traitement topique ciblé du bord de la paupière pour des patients présentant des épisodes aigus de blépharite, une pathologie courante de l'oeil caractérisée par une inflammation de la paupière. NCX 4251 sera administré à l'aide d'un bâtonnet applicateur sur le bord de la paupière directement au niveau du site inflammatoire, minimisant ainsi une potentielle pénétration du médicament au travers de la cornée, laquelle peut provoquer des effets secondaires dommageables, tels qu'une augmentation de la pression intraoculaire, identifiés avec les stéroïdes topiques actuels.
Le propionate de fluticasone, le principe actif du NCX 4251, qui n'a pas fait l'objet d'une précédente utilisation dans une formulation topique ophtalmique approuvée, présente une affinité pour les récepteurs aux glucocorticoïdes environ 10 fois supérieure à celle de la dexaméthasone, un corticostéroïde couramment utilisé en ophtalmologie. La fluticasone est un glucocorticoïde possédant de puissantes propriétés anti-inflammatoires qui a été approuvé dans de nombreuses spécialités médicamenteuses au cours des 20 dernières années pour le traitement d'indications diverses comprenant des affections dermatologiques, la rhinite et l'asthme.
La blépharite - un marché inexploité
La blépharite est une affection caractérisée par une rougeur et un gonflement du bord des paupières, potentiellement accompagnée de desquamations. 37% et 47% des patients, consultant un ophtalmologiste et un optométriste respectivement, présentent des symptômes de cette maladie.
Il n'existe actuellement aucun médicament sur prescription approuvé par la FDA américaine pour la blépharite spécifiquement. Les ventes annuelles aux Etats-Unis des produits prescrits pour la blépharite représentent une valeur totale de plus de 500 millions de dollars selon IQVIA Health Analytics. Les études révèlent que les ophtalmologistes considèrent l'activité anti-inflammatoire comme la propriété la plus importante d'un produit dans le choix d'un traitement pour de la blépharite, ce qui milite en faveur du développement du NCX 4251.
A propos de Nicox
Nicox S.A. est une société internationale spécialisée en ophtalmologie développant des solutions innovantes visant au maintien de la vision et à l'amélioration de la santé oculaire. S'appuyant sur son expertise exclusive en matière de libération d'oxyde nitrique (NO) et d'autres technologies, la Société développe un large portefeuille de nouveaux candidats médicaments ciblant de multiples pathologies oculaires, dont le glaucome. Le portefeuille de Nicox comprend trois programmes en développement incluant NCX 470 pour la réduction de la pression intraoculaire issu de sa plateforme de recherche de composés donneurs de NO brevetés et NCX 4251, une formulation brevetée de la molécule fluticasone d'usage bien établi, pour les épisodes aigus de blépharite. Les activités de recherche de Nicox sont concentrées sur de nouveaux donneurs de NO de future génération comprenant les donneurs de NO inhibiteurs de la phosphodiestérase-5 (PDE-5) et les donneurs de NO stimulateurs de la guanylate cyclase soluble (sGC) en partenariat avec Ironwood. De plus, Nicox a deux produits ophtalmiques approuvés par la Food and Drug Administration (FDA) américaine : VYZULTA ® (solution ophtalmique de latanoprostène bunod), 0,024%, licencié exclusivement au niveau mondial à Bausch + Lomb, une société de Bausch Health Companies Inc., et commercialisé aux Etats-Unis par le partenaire depuis décembre 2017 ainsi que ZERVIATE(TM) (solution ophtalmique de cétirizine), 0,24%, licencié exclusivement aux Etats-Unis à Eyevance Pharmaceuticals. Nicox, dont le siège social est à Sophia Antipolis (France), est cotée sur Euronext Paris (Compartiment B : Mid Caps ; Mnémo : COX) et fait partie des indices CAC Healthcare, CAC Pharma & Bio et Next 150.
Pour plus d'informations sur Nicox, ses produits ou son portefeuille : www.nicox.com
Couverture par les analystes
Bryan, Garnier & Co Hugo Solvet Paris, France
H.C. Wainwright & Co. Yi Chen New York, Etats-Unis
Les positions exprimées par les analystes dans leurs notes sur Nicox leurs sont propres et ne reflètent pas celles de la Société. De plus, les informations contenues dans leurs rapports peuvent ne pas être correctes ou à jour. Nicox s'affranchit de toute obligation de corriger ou de mettre à jour les informations contenues dans les rapports des analystes.
Prochaines conférences investisseurs et business
19-20 mars Oppenheimer's 29th Annual Healthcare Conference New York, Etats-Unis
7-9 avril H.C. Wainwright Global Life Sciences Conference London, Royaume-Uni
16-17 avril SmallCap Event Paris, France
16 mai European MidCap Event Copenhague, Danemark
2-6 juin BIO 2019 Philadelphie, Etats-Unis
18-19 juin European MidCap Event Paris, France
19-20 juin JMP Securities Healthcare Conference New York, Etats-Unis
Contacts
Nicox
Gavin Spencer,
Executive Vice President, Chief Business Officer
& Head of Corporate Development
T +33 (0)4 97 24 53 00
[email protected]
Relations Investisseurs & Média
Etats-Unis et Europe
LifeSci Advisors, LLC
Hans Herklots
T +41 79 598 71 49
[email protected] Relations Média
France
LifeSci Advisors, LLC
Sophie Baumont
M. +33 (0)6 27 74 74 49
[email protected]
Avertissement
Les informations contenues dans le présent document pourront être modifiées sans préavis. Ces informations contiennent des déclarations prospectives, lesquelles ne constituent pas des garanties quant aux performances futures. Ces déclarations sont fondées sur les anticipations et les convictions actuelles de l'équipe dirigeante de Nicox S.A. et sont tributaires d'un certain nombre de facteurs et d'incertitudes en conséquence desquels les résultats réels pourraient sensiblement différer de ceux décrits dans les déclarations prospectives. Nicox S.A. et ses affiliés, administrateurs, dirigeants, employés, conseils ou mandataires ne prennent pas l'engagement et ne sont pas tenus de publier des mises à jour d'une quelconque déclaration prospective ou de réviser une quelconque déclaration prospective.
Les facteurs de risque susceptibles d'avoir des répercussions significatives sur l'activité de Nicox S.A. sont exposés au chapitre 4 du Document de référence, rapport annuel et rapport de gestion 2018 qui a été déposé auprès de l'AMF le 6 mars 2019 et qui est disponible sur le site de Nicox (www.nicox.com).
Nicox S.A.
Drakkar 2
Bât D, 2405 route des Dolines
CS 10313, Sophia Antipolis
06560 Valbonne, France
T +33 (0)4 97 24 53 00
F +33 (0)4 97 24 53 99
Communiqué de presse
This announcement is distributed by West Corporation on behalf of West Corporation clients.
The issuer of this announcement warrants that they are solely responsible for the content, accuracy and originality of the information contained therein.
Source: NICOX via Globenewswire
15/03/2019 | 07:30 Signature d'un accord sur ZERVIATE pour la Chine. Paiements d'étape et redevances pouvant atteindre 17 millions d'euros
Communiqué de presse
15 mars 2019 - diffusion à 7h30
Sophia Antipolis, France
Nicox SA (Euronext Paris : FR0013018124, COX, éligible PEA-PME), une société internationale spécialisée en ophtalmologie, annonce aujourd'hui avoir conclu un accord de licence exclusif avec Ocumension Therapeutics pour le développement et la commercialisation de son produit, ZERVIATETM (solution ophtalmique de cetirizine), 0,24%, pour le traitement des conjonctivites allergiques sur un territoire comprenant la Chine continentale, Hong Kong, Macao et Taiwan. Nicox et Ocumension ont récemment conclu une autre collaboration sur le même territoire pour le développement et la commercialisation de NCX 470 pour les patients atteints de glaucome ou d'hypertension oculaire. Ocumension Therapeutics est une société d'ophtalmologie financée par 6 Dimensions Capital, l'un des fonds d'investissement de premier plan au niveau mondial dans le domaine de la santé, issu de la fusion de Wuxi Healthcare Ventures et de Frontline BioVentures.
Nicox a concédé à Ocumension les droits exclusifs de développement et de commercialisation de ZERVIATE dans le territoire précité. Selon les termes de l'accord, Nicox pourrait potentiellement recevoir d'Ocumension des paiements d'étape liés au développement et aux ventes d'un montant pouvant atteindre jusqu'à 17 millions d'euros ainsi que des redevances échelonnées de 5% à 9% sur les ventes de ZERVIATE.
"Suite à notre collaboration pour NCX 470, le choix d'Ocumension pour licencier ZERVIATE dans cette région était évident" a déclaré Gavin Spencer, Chief Business Officer de Nicox. "Nicox, qui a à son actif plusieurs partenariats, est activement engagé dans des discussions pour maximiser la valeur de ses actifs au stade commercial et en développement en dehors des marchés américain et européen. Nous espérons donc annoncer d'autres collaborations internationales pour ZERVIATE dans les mois à venir."
"ZERVIATE apporte à Ocumension un produit supplémentaire à un stade avancé qui élargit notre domaine thérapeutique à l'allergie oculaire" a déclaré Ye Liu, Président directeur général d'Ocumension. "Nous apprécions beaucoup la collaboration avec Nicox et cet accord renforce nos relations avec l'une des principales sociétés de R&D dans le domaine de l'ophtalmologie."
Ocumension prévoit que des études cliniques supplémentaires devront être menées pour l'approbation réglementaire de ZERVIATE sur le marché chinois. Toutes les activités de développement seront supervisées par un Comité de Développement Conjoint comprenant des représentants des deux sociétés, Ocumension étant responsable de toutes les activités à ses propres frais.