• L'OBESITE : UN BESOIN INSATISFAIT
Selon le Journal international de l'obésité, le phénomène d'excès de poids et d'obésité touche 21,8 % de la population dans le monde (Source : CNS) et coûte pour les seuls Etats-Unis près de 150 Milliards de dollars par an en dépenses publiques.
En France, l’obésité touche 20,6% des hommes et 20,8% des femmes (Source : InstitutPasteur). Chez les 35-74 ans, l’étude montrait même que "67 % des hommes et 50 % des femmes présentent une surcharge pondérale ou une obésité". Une autre étude française montrait que l’obésité avait augmenté de 50% en 10 ans (Source : Cite Sciences).
Face à ce fléau, il n'existe pas de véritable alternative médicamenteuse : le régime alimentaire et l'exercice physique sont la norme pour aider les gens à perdre du poids. Mais certains font état que ces efforts sont souvent si difficiles que les médicaments ou d'autres options comme la chirurgie sont alors nécessaires.
• L'OPTION THERAPEUTIQUE D'OREXIGEN POUR TRAITER L'OBESITE
Deux comprimés deux fois par jour pour perdre au moins 5% de son poids, sans connaître d'effets indésirables : la pilule miracle de la Biotech OREXIGEN aurait-elle ces vertus ? Enjeu : des ventes annuelles qui pourraient atteindre 1,2 milliards $ d'ici 2018 (selon les données de BioMedTracker) contre seulement 382 millions $ en 2009 (selon IMS Health). Avant le vote positif en faveur d'Orexigen, plusieurs sociétés avaient subi un échec. Tel que je l'ai détaillé dans mon article du mois de Septembre, pas moins de quatre sociétés se sont vues refuser ou retirer du marché leur médicament en 2010 (Sanofi, Abbott, Vivus et Arena). Aussi, j'ai choisi de vous montrer un comparatif entre les trois Biotechs qui ont présenté un dossier en vue d'une approbation pour rafler la mise sur le juteux marché de l'obésité (Orexigen, Arna et Vivus).
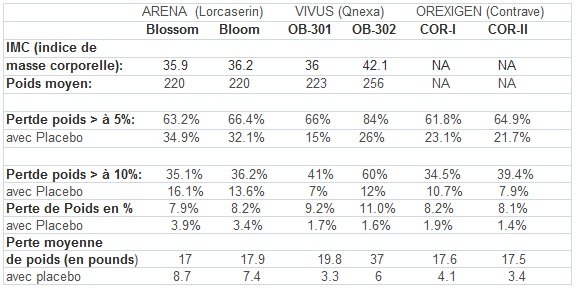
Sources pour les données : résultats des Etudes (BLOOM Data / BLOSSOM Data / Vivus Data / Orexigen Data I / Orexigen Data II).
Le comité d'experts de la FDA a donc voté à l'unanimité le 7 Décembre (à 13 voix contre 7) pour que le Contrave de la Biotech OREXIGEN (OREX) soit mis sur le marché. Selon le Panel d'experts, les avantages de perte de poids observée avec Contrave l'emportent sur la sécurité du médicament (préoccupations des risques cardiaques). Michael Narachi, président et chef de la direction d' Orexigen a déclaré suite à ce vote : "nous nous sommes engagés à travailler pour fournir de nouvelles options thérapeutiques dans la gestion de l'obésité et aider les médecins pour réduire cette épidémie. Nous croyons que le Contrave, si il est approuvé, pourrait être une alternative importante aux options thérapeutiques limitées qui sont actuellement disponibles."
En matière d'approbation d'un médicament, la clé de la réussite est un bon compromis bénéfice/risque. rexigen avait mis en avant qu'une perte de poids, même modeste, pouvait améliorer considérablement la santé d'un patient en réduisant le risque pour les maladies chroniques liées à l'obésité comme le diabète et les maladies cardiaques. A propos du bénéfice : comme nous le montre ce tableau, le Contrave d'Orexigen n'était pas plus efficace. Il était en ligne par rapports à ses deux concurrents. Disons que le Contrave remplissait les critères d' efficacité de la FDA : au moins 35 % des patients étudiés ont perdu au moins 5 % de leur poids (le double du placebo).
La grande différence vient en fait des risques (effets secondaires). Aux vues des effets indésirables, le panel consultatif de la FDA a jugé que le Contrave disposait d'une bonne sécurité. Il faut dire que le Contrave disposait d'un avantage certain : ce médicament est un cocktail de deux molécules déjà approuvées, ce qui allait jouer en sa faveur : le bupropion, un antidépresseur également utilisé pour cesser de fumer, et le naltrexone, un traitement de l'alcoolisme et de la toxicomanie.
Avant cette annonce du 7 Décembre, la principale interrogation résidait dans le fait de savoir si OREXIGEN pouvait réussir là où ses rivaux avaient échoué, pour exploiter le marché de l'obésité.Les analystes de JP Morgan n'ont pas manqué de souligner le point crucial sur lequel le comité consultatif de la FDA allait devoir statuer : "il est clair que la discussion sur la sécurité sera une fois de plus la clé, en particulier en ce qui concerne le risque cardiovasculaire" ont précisé les analystes à Reuters avant le verdict de la FDA. C'est aussi ce que j'avais soulevé au mois de Septembre dans mon article initial.
• TOUT N'EST PAS ENCORE GAGNE POUR OREXIGEN
L'approbation du Contrave d'Orexigen a pris de cours de nombreux observateurs. Ce fut le cas d'Elemer Piros, analyste chez Rodman & Renshaw (selon moi, R&R est le broker qui est le plus performant en matière de suivi des sociétés Biotechs), qui ne cachait pas son pessimisme sur le dossier. Piros estimait le 3 Décembre dans les colonnes de Bloomberg qu' Orexigen pouvait être amené à faire une étude approfondie sur les effets cardiovasculaires avant une approbation définitive. L'analyste avait alors un objectif de prix de 2 $ alors que le cours cotait 5$. Une autre question soulevée était de savoir si les données sur 12 mois étaient suffisantes pour un médicament dont les critiques sont nombreuses et qui sera utilisé sur une plus large durée par de très nombreux patients.
Certains experts ont aussi émis quelques réserves sur le Contrave, y compris certains ayant voté pour l'approbation. Michael Rogawski, un neurologue à l'Université de Californie a avancé à Reuters : « je me sens le promoteur a rencontré les exigences de la FDA... D'autre part, je pense que c'est un produit très imparfait ». La FDA et Orexigen sont encore en pourparlers au sujet d'un autre essai pour examiner de plus près les problèmes cardiaques potentiels et les effets cardio-vasculaires. Les risques cardiaques, les convulsions et les comportements suicidaires seront donc à suivre de près en matière de sécurité.
Pour l'heure, la FDA n'a pas encore confirmé l'autorisation de mise sur le marché (le comité d'expert est juste un panel consultatif). Mai d'après mon expérience, la FDA suit généralement les recommandations du comité (dans 80% des cas environ). La FDA doit se prononcer sur sa décision finale le 31 janvier prochain pour valider la mise sur le marché. Tout n'est pas encore acquis, puisque la FDA peut très bien limiter l'accès à ce médicament avec des contre indications, ce qui impacterait les ventes du Contrave.
Le prochain catalyseur de la hausse est la date du 31 Janvier 2011, qui sera déterminante (à cette date, nous connaîtrons la décision définitive de la FDA sur l'approbation du Contrave).
• CONCLUSION – EXPERIENCE DE TRADING
OREXIGEN était un pari risqué, car cette Biotech se concentre uniquement sur les médicaments contre l'obésité et n'a pas de produits sur le marché. Aussi, la barre était placée très haute par la FDA, puisque plusieurs médicaments anti obésité avaient été refusé ou retiré du marché.
Le risque sur ce dossier était très présent. Un échec du Contrave lui aurait porté un sérieux coup. Avec cette bonne nouvelle, le marché a pris en considération le marché potentiel qui se dessine pour OREXIGEN. Ce 8 Dècembre, on assiste à une très forte hausse (+115% à mi-séance) dans des volumes très conséquents (30% du Capital échangé à mi-séance).
Pour autant, par mesure de sécurité : j'ai vendu la moitié de ma position avant l'approbation. Avec un prix de revient de 5,50 $, je me frotte les mains, sans paniquer. Je décide de vendre ¼ aux abords des 11$. Je décide de conserver le solde (¼ de ma pose initiale) pour le Long terme : pour profiter de la sous-valorisation d'OREXIGEN qui vaut ce jour 500 Millions $, alors qu'on attend des ventes de plus de 1 milliard de $ par an, rien qu'aux Etats-Unis. Ce chiffre suffit à lui seul pour justifier du potentiel d'appréciation que recèle cette action pour les prochaines années si tout se passe bien.
Sacha Pouget
