que passa ? Cours temps réel: 0,888 22,15%
Je suis rentré tard et pas déçus.
Bravo aux cou il les durs qui avaient tenu
belle clôture tout de même ! Cours temps réel: 0,63€ 18,42%
Cours temps réel: 0,599€ 12,59% ?
La configuration graphique est vérifiée.
N'oublions pas le contexte, la prise de PV est recommandée.
*: Non actionnaire
------------------
Cours temps réel: 0,756€ 13,34%
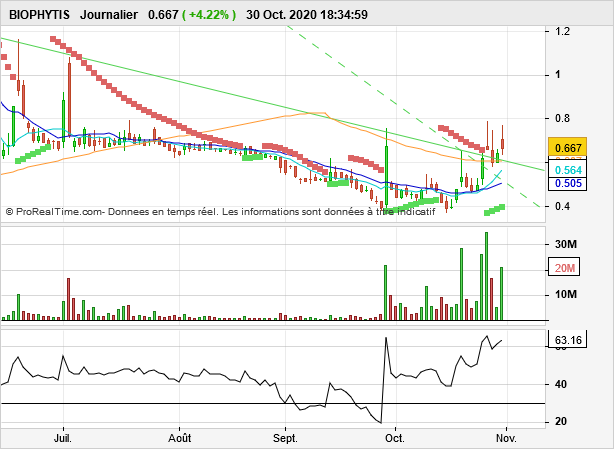
La configuration graphique en journalier:
Message complété le 01/11/2020 08:28:08 par son auteur.
Support Oblique, SAR vert polarité inversée, volumes présents, RSI convergent vers le nord...à confirmer
Prudence de mise valeur spéculative. Bons trades
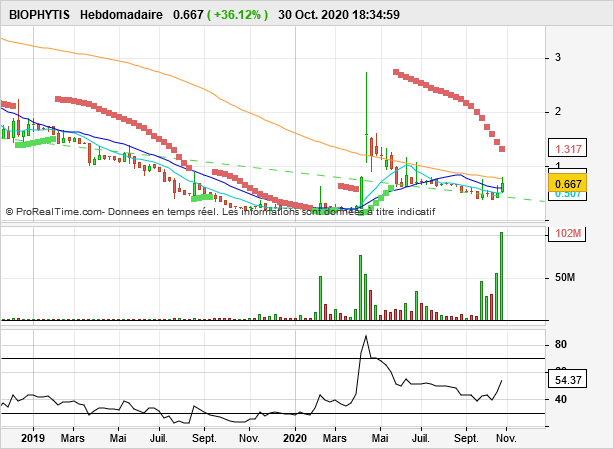
La configuration Graphique Hebdomadaire
Message complété le 01/11/2020 08:24:43 par son auteur.
Support Oblique touché, SAR rouge en inversion de polarité, et RSI convergent, direction nord...reste à confirmer
Message complété le 01/11/2020 10:56:09 par son auteur.
Lire: Volumes et RSI convergent
Cours temps réel: 0,754€ 17,81% ?
La total mdr
Cours temps réel: 0,693€ 75,00%
si on ne casse passe pas les 0,74 on peut vendre pour se repositionner plus bas
ca va ramasser sec avant vendredi positionnez vous avant rush semaine pro
Testing the Efficacy and Safety of BIO101 for the Prevention of Respiratory Deterioration in COVID-19 Patients (COVA)
The safety and scientific validity of this study is the responsibility of the study sponsor and investigators. Listing a study does not mean it has been evaluated by the U.S. Federal Government. Know the risks and potential benefits of clinical studies and talk to your health care provider before participating. Read our disclaimer for details.
ClinicalTrials.gov Identifier: NCT04472728
Recruitment Status : Recruiting
First Posted : July 15, 2020
Last Update Posted : July 15, 2020
See Contacts and Locations
Sponsor:
Biophytis
Information provided by (Responsible Party):
Biophytis
Ça recommence à charge on pourrait initier retours au 1 euros
Si ça fonctionne ça sera le 50 ème trad gagnant de mars
On va souffler les bougies
Voir les nouveaux Tweets
Conversation
Okim59
@okim59
Biophytis $ALBPS
Index pointant vers la droite We are confident that the beneficial effects of 20E/BIO101 will also be further established on e.g. lungs, kidneys and cardiovascular pathologies and could offer new therapeutic strategies
https://biorxiv.org/content/10.1101/2020.04.08.032607v1.full.pdf
8:14 AM · 14 juil. 2020·Twitter for iPad
2
Retweets
3
J'aime
Titi Valk
@TitiValk
·
2h
En réponse à
@okim59
1/2resultats impressionnants sur les souris ( présentés également dans le Doc Corporate de Juin ) qui a incité des institutionnels a investir 10 M d'euros dans #biophytis. les brevets validés par le #WIPO dans ce mecanisme sécurisent la valeur de l'entreprise!
Titi Valk
@TitiValk
·
2h
2/2 ce sont également ces données cliniques qui ont permis a #biophytis de mettre sur pied le protocole d'etude clinique de #COVA dans la #SDRA liée a #COVID19.
recepteur MAS! tout est lié en cas de reussite #COVA #SARA dans la sarcopénie et #MYODA
Brief Summary:
The SARA-OBS is a single arm phase 2 clinical trial, with no investigational product and no therapeutic intervention that will be conducted in three European countries, (Belgium, France and Italy), and in the US.
300 community dwelling older adults (men or women≥65 years) reporting loss of physical function and at risk of mobility disability, will undergo mobility functional evaluation and Dual-energy X-ray Absorptiometry DXA scan for body composition determination twice, at six-month interval.
Participants aged ≥ 65 years complaining of poor physical function will be selected to perform SPPB (Short Physical Performance Battery)tests. Those with SPPB scores ≤ 8/12 will be selected to perform body composition analysis with DXA Scan. Participants with ALM/BMI < 0.789 in men and 0.512 in women will be included. The investigational phase will comprise two main visits: the inclusion visit and the 6-month visit. Both the 6-minute walk distance test and the 400-metre walking test will be administered at the main visits. Patient Reported Outcomes (PROs) will be completed by the patients at the same visits.
Condition or disease Intervention/treatment
Sarcopenia Gait Disorders in Old Age Muscle Weakness Other: No Drug and no aspecific intervention
Detailed Description:
The SARA-OBS is a phase 2 clinical trial, with no investigational product and no therapeutic intervention. It will be conducted in three European countries, Belgium, France and Italy, and in the US.
300 community dwelling older adults (men or women≥65 years) reporting loss of physical function and at risk of mobility disability, will undergo mobility functional evaluation and Dual-energy X-ray Absorptiometry DXA scan for body composition determination twice, at six-month interval.
The general objective is to characterise sarcopenia including "sarcopenic obesity" in a population of older persons living in the community and at risk of mobility disability; evaluate their physical performance and body composition in view of the design of a phase 2 clinical study on the efficacy and safety of BIO101 on the prevention of mobility disability in the at-risk community dwelling older adults (≥65 years) reporting loss of physical function.
The primary objective characterise sarcopenia including sarcopenic obesity, in older persons at risk of mobility disability. Sarcopenia will be defined according to the criteria of the Foundation of NIH; the risk of mobility disability will be operationalised by the Short Physical Performance Battery (SPPB). For this purpose, the 6-minute walking distance and the 400-meter walking test will be evaluated at 6-month intervals, in the absence of any therapeutic intervention. The incident rate of change will be estimated on the sample and pre-specified subgroups (e.g. gender, SPPB baseline score, etc.).
Two important Secondary Objectives are also included :
To evaluate muscle strength (handgrip/knee extension) and stair power climbing test
To evaluate self-administered quality-of-life tests as putative patient reported outcomes (PROs): Short Form Health Survey (SF-36) and Sarcopenia Quality of Life (SarQol) for all subjects; in addition, TSD-OC for participants with BMI≥30
Exploratory objectives are :
To measure tentative biomarkers of sarcopenia and poor physical performance, and test their correlation with physical function change over the study observation.
To record actimetry via a connected wearable device, in order to describe daily physical activity and possibly identify patterns predictive of improvement/worsening of physical function.
Primary endpoints are the 6-minute Walk Test/400m Walking Test and Co-Primary endpoints are SF-36 and SarQoL for all subjects; additionally TSD-OC for subjects with BMI ≥ 30.
Study Design
Go to
Study Type :
Observational
Actual Enrollment :
218 participants
Observational Model:
Cohort
Time Perspective:
Prospective
Official Title:
Characterising SARcopenia and Sarcopenic Obesity in Patients Aged 65 Years and Over at Risk of Mobility Disability. An OBServational Clinical Trial (SARA-OBS)
Actual Study Start Date :
February 8, 2017
Actual Primary Completion Date :
November 30, 2019
Actual Study Completion Date :
June 30, 2020
Groups and Cohorts
Go to
Intervention Details:
Other: No Drug and no aspecific intervention
No intervention
Outcome Measures
Go to
Primary Outcome Measures :
6-minute or 400 meters walk. [ Time Frame: Change from Baseline 6 minute or 400 meters to measurement at 6 months. ]
The 6 minutes walking distance is a functional exercise capacity test that involves measuring the distance covered by a participant within a specified time of 6 minutes. The 400 meter walking test is a measure of how long it will take for a volunteer to complete the specified 400 meters distance.
Secondary Outcome Measures :
SPPB [ Time Frame: Change from Baseline SPPB to measurement at 6 months. ]
Physical performance tests corresponding to standing balance, walking speed and chair stand will be assessed
DEXA [ Time Frame: Change from Baseline DEXA to measurement at 6 months. ]
Body composition especially Lean Body Mass and Fat Mass will be measured. This will allow definition of the appendicular Lean Body mass.
Stair Climb Power Test [ Time Frame: Change from Baseline Stair Climb Power Test to measurement at 6 months. ]
The ability to ascend and descend stairs (9 stairs of 20 cm height) will be assessed in a specific period of time
Actimetry [ Time Frame: Change from actimetry at Month1 to measurement at 6 months. ]
The continuous physical activity of the volunteers will be recorded using a specific device during the 6-month study period.
Grip strength [ Time Frame: Change from Baseline Grip Strength to measurement at 6 months. ]
The grip strength will be measured using the appropriate dynamometer. Strength will be measured 3 times for both hands and the highest value will be kept for further analysis.
Knee extension [ Time Frame: Change from Baseline knee extension to measurement at 6 months. ]
The knee extension measurement will be performed using isokinetic dynamometer.
Patient Reported Outcome : SF-36 [ Time Frame: Change from Baseline Patient Reported Outcome to measurement at 6 months. ]
Electronically self administrated Patient Reported Outcome SF-36 will be assessed a SF-36 questionnaire.
Patient Reported Outcomes : SarQoL [ Time Frame: Change from Baseline Patient Reported Outcome to measurement at 6 months. ]
Electronically self administrated Patient Reported Outcome SarQoL will be assessed through the SarQoL questionnaire.
Patient Reported Outcomes TSC-OD for patients with BMI>30 [ Time Frame: Change from Baseline Patient Reported Outcome to measurement at 6 months. ]
Electronically self administrated Patient Reported Outcomes will be assessed through the TSD-OC questionnaire for volunteers having BMI>30
Patient Reported Outcomes (PAT-D) [ Time Frame: Change from Baseline Patient Reported Outcome to measurement at 6 months. ]
Electronically administrated Patient Reported Outcome will be assessed with assistance of the investigator through the PAT-D questionnaire.
Biomarkers [ Time Frame: Change from Baseline Biomarkers to measurement at 6 months ]
Biomarkers specific to Sarcopenia and to the Renin Angiotensin System ( Aldosterone; Renin; Myostatin; PIIINP; IL-6; hsCRP etc....) will be measured at baseline and at 6 months.
Attention nouveau trad en vu sur biophytis
https://clinicaltrials.gov/ct2/show/NCT03021798?term=Biophytis&draw=2&rank=2
01/07/2020 | 22:32
Biophytis annonce l'émission d'une tranche d'ORNANE d'un montant de 3 millions d'euros
Paris (France), Cambridge (Etats-Unis), 1er juillet 2020, 21h00- BIOPHYTIS (Euronext Growth Paris : ALBPS), société de biotechnologie au stade clinique, spécialisée dans le développement de candidats médicaments pour le traitement des maladies liées à l'âge, notamment les maladies neuromusculaires, annonce aujourd'hui l'émission de 120 Obligations Remboursables en Numéraire ou en Actions Nouvelles ou Existantes (ORNANE), d'une valeur nominale totale de 3 millions d'euros. Cette seconde tranche de financement d'Atlas va permettre à Biophytis de poursuivre le développement de Sarconeos (BIO101) pour le traitement de la sarcopénie (étude SARA-INT de phase 2b) et d'insuffisance respiratoire aiguë liée au Covid-19 (étude COVA de phase 2/3).
suite Z B
Biophytis a annoncé le 7 avril 2020 la mise en place d'une ligne de financement pouvant atteindre 24 millions d'euros levée auprès d'Atlas, un fond d'investissement spécialisé basé à New York (Etats-Unis), et prévoyant l'émission de 960 ORNANE, d'une valeur nominale de 25.000 euros chacune. Le financement de 24 millions d'euros est étendu en 8 tranches de 3 millions d'euros chacune sur une durée totale de 3 ans, sans obligation de tirage. La Société a tiré une première tranche de 3 millions d'euros au cours du mois d'avril 2020. La société a fait usage de la faculté qu'elle a, au titre du contrat, de demander à Atlas la suspension des conversions, pour une période allant du 1er au 31 juillet 2020.
Message complété le 02/07/2020 00:06:44 par son auteur.
Biophytis : reçoit l'accord de la FDA pour démarrer l'essai clinique COVA de phase 2/3 avec Sarconeos (BIO101) dans le traitement de l'insuffisance respiratoire liée au COVID-19. Lire le communiqué de presse
share with twitter share with LinkedIn share with facebook
0
01/07/2020 | 22:32
Biophytis reçoit l'accord de la FDA pour démarrer l'essai clinique COVA de phase 2/3 avec Sarconeos (BIO101) dans le traitement de l'insuffisance respiratoire liée au COVID-19
Paris (France), Cambridge (Etats-Unis), 1 juillet 2020, 21h00- BIOPHYTIS (Euronext Growth Paris : ALBPS), société de biotechnologie au stade clinique, spécialisée dans le développement de candidats médicaments pour le traitement des maladies liées à l'âge, notamment les maladies neuromusculaires, annonce aujourd'hui avoir reçu l'accord de la US Food and Drug Administration (FDA) lui permettant de démarrer son programme de développement clinique : COVA. Le programme clinique COVA, une étude de phase 2/3, va évaluer Sarconeos (BIO101) dans le traitement potentiel de l'insuffisance respiratoire aiguë associée au COVID-19.
Le programme COVA consiste à évaluer l'efficacité et l'innocuité de Sarconeos (BIO101) dans le traitement de la détérioration de la fonction respiratoire des patients présentant des symptômes respiratoires sévères associés au COVID-19. Cet essai clinique international clé, se déroulera en deux parties. La première partie a pour objectif d'évaluer l'innocuité du traitement et de fournir une indication sur l'activité de Sarconeos (BIO101) chez 50 patients hospitalisés atteints du COVID-19 souffrant d'insuffisance respiratoire aiguë. Une deuxième partie, avec environ 300 patients supplémentaires, étudiera l'efficacité de Sarconeos (BIO101) sur la f
oui c est bien camarade.
les millionaires pousses comme des pâquerettes sur ABC.
