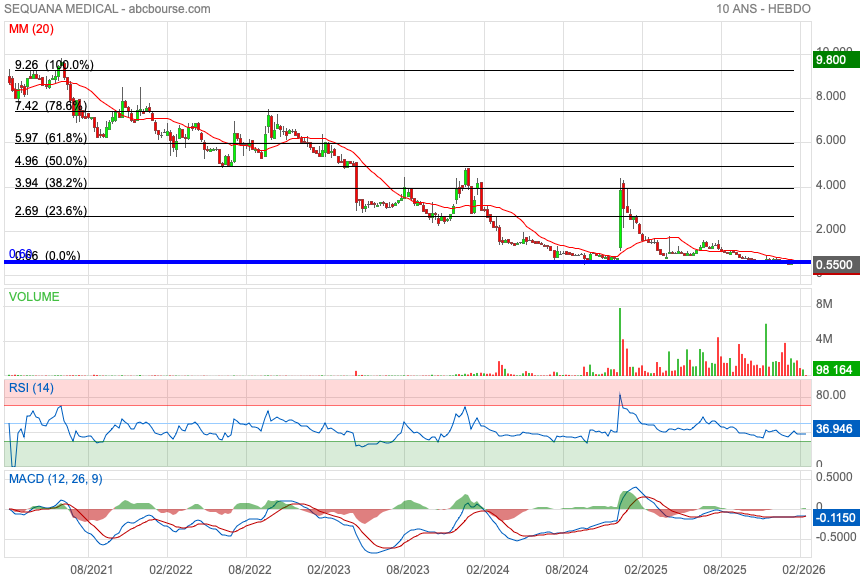
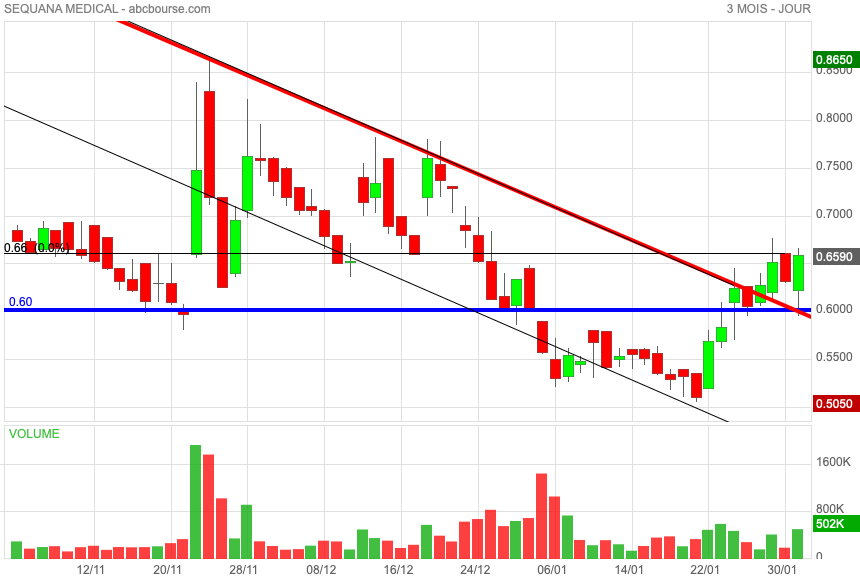
La société aurait demandé à euronext Bruxelles de suspendre la cotation . La publication des résultats prévue le 28 avril n'a pas eu lieu et a été différée.
ABM FN) Sequana Medical évalue ses options financières et stratégiques au regard de sa situation financière actuelle et de l'avenir de l'entreprise. C'est ce qu'a annoncé la société ce mardi soir.
Cette évaluation est menée avec l'aide de conseillers et pourrait déboucher sur des accords de financement ou une transaction stratégique concernant la société ou ses actifs, a déclaré Sequana.
Compte tenu de cette évaluation, les rapports financiers de l'année écoulée ne seront pas encore disponibles lors de l'assemblée générale annuelle du 28 mai. Le conseil d'administration propose donc de traiter les résultats à une date ultérieure.
Le conseil d'administration a constaté que les capitaux propres nets sont négatifs, sur la base des informations financières provisoires relatives à 2025.
En l'absence d'un rapport financier définitif, Sequana a demandé à l'autorité de surveillance des marchés financiers (FSMA) de suspendre la cotation de l'action.
Mon avis personnel qui ne tient qu'à moi : rachat du groupe par Medtronics.
Et à ce moment là, les 80 millions d'actions vaudront la somme décidée pour la rachat divisé par 80 Millions.
Si sequana médical est racheté à 80 Millions d:euros , l'action vaudra 1€.
Message complété le 29/04/2026 05:08:14 par son auteur.
Selon chatgpt, un cours entre 1,20 et 1,50!€ , voire 2,5€ pourrait être possible
Message complété le 30/04/2026 04:12:47 par son auteur.
On doit désormais attendre la suite des évènements, mais je reste positif sur le sort de la société, alors que certains envisagent une dilution extrêmement douloureuse.
Message complété le 06/05/2026 07:21:50 par son auteur.
6 sitesSi l'on compare la situation de Sequana Medical à des acquisitions récentes de medtechs en difficulté (entre 2024 et 2026), on observe que le prix final de rachat dépend moins du cours de bourse que de la valeur stratégique des actifs (brevets FDA, technologie).Voici comment affiner l'estimation d'un prix de rachat potentiel par un acteur comme Medtronic :1. Références de rachat d'actifs "sous pression" (2024-2026)Prime sur le cours : Dans le cas d'Aerie Pharmaceuticals (racheté par Alcon), la prime était de 37 % sur le dernier cours. Pour Sequana, avec un dernier cours à 0,61 €, une prime similaire porterait le prix à environ 0,84 €.Acquisitions de "niche" par Medtronic : Medtronic a récemment finalisé le rachat de CathWorks (avril 2026) pour 585 millions de dollars et de Scientia Vascular pour 550 millions de dollars. Ces sociétés, bien que mieux financées que Sequana, montrent que Medtronic est prêt à payer des montants significatifs pour des technologies cardiovasculaires ou de gestion des fluides validées.2. Estimation de prix pour Sequana MedicalEn tenant compte de la position de faiblesse financière actuelle (capitaux propres négatifs) mais de la valeur de l'approbation FDA, deux scénarios se dessinent :Scénario "Sauvetage" (Prix bas) : entre 0,75 € et 1,10 € par action.C'est le scénario le plus probable si Medtronic rachète la société avant une éventuelle faillite. Le prix couvre les dettes et offre une petite prime aux actionnaires actuels pour éviter une bataille judiciaire.Scénario "Potentiel technologique" (Prix moyen) : entre 1,50 € et 2,00 € par action.Ce prix correspondrait à la valeur estimée par les analystes avant la crise de liquidité (comme Jefferies ou Degroof Petercam). Ce montant serait justifié par le marché potentiel de 2,4 milliards de dollars de l'alfapump aux États-Unis.3. La structure "Earn-out" : une probabilité forteIl est très fréquent que les grands groupes comme Medtronic proposent un prix de rachat initial faible, complété par des paiements conditionnels.Exemple : 0,80 € par action immédiatement + 1,00 € supplémentaire si Sequana atteint 500 implantations aux États-Unis en 2027. Cette structure permet à l'acheteur de ne pas surpayer un actif risqué.Conclusion : Un rachat immédiat se situerait probablement dans une fourchette de 0,80 € à 1,20 €, très loin des sommets historiques du titre, mais offrant une porte de sortie honorable dans le contexte de suspension actuelle.
La publication du rapport annuel 2025 de Sequana Medical est officiellement prévue pour aujourd'hui, le 28 avril 2026.
Sequana Medical
D'après les calendriers financiers spécialisés, la diffusion est généralement attendue :
Vers 07h00 (CEST), soit avant l'ouverture de la bourse d'Euronext Bruxelles.
Certains rapports financiers précédents ont également été publiés après la clôture du marché ou tard le soir (vers 22h00 CEST), mais la tendance pour les résultats annuels privilégie une annonce matinale.
À cette heure, un communiqué de presse détaillé devrait être disponible sur la page des communiqués de Sequana Medical et sur le portail Euronext.
Message précédent écrit ce matin à 8h28
Marrant de voir la spéculation à la veille de la publication des résultats 2025.
Volume et hausse ?
La prudence est de mise néanmoins.
On connaît parfois des -25% ou -30% par la suite.
74% de perte , mais toujours confiant !
Résultats le 28 avril 2026 pour l'année 2025.
Cotee chez nos amis belges.
Rendez vous en ...2030
De quoi parle t on ?
Sequana Medical (Euronext: SEQUA) progresse dans la commercialisation de son alfapump® aux États-Unis, avec cinq centres ayant réalisé des implants début 2026. La société, focalisée sur la surcharge fluidique, a sécurisé des financements (dont un accord GEM) pour soutenir le lancement et le développement du DSR (Direct Sodium Removal).
Sequana Medical
Sequana Medical
+3
Voici les points clés récents :
Commercialisation US : L'alfapump, dispositif pour la cirrhose, est en cours de déploiement aux USA.
Financement : Des levées de fonds (24 M€ en 2025) ont été sécurisées pour étendre les opérations.
Pipeline DSR : Poursuite du développement du DSR 2.0 pour l'insuffisance cardiaque, incluant l'étude MOJAVE.
Finances 2025 : Réduction des dépenses cliniques, notamment en différant le démarrage de la phase randomisée de MOJAVE.
Action : Le cours est sous pression, mais la société fait l'objet de suivis prometteurs.
Sur le site de la société
Message complété le 27/04/2026 14:40:18 par son auteur.
Si des résultats intéressants étaient publiés demain , ce pourrait être un emballement sur le titre . Certains en tout cas achètent aujourd'hui.
Pari risqué ?
Réponse demain avec la publication
Merveilleux, la pépite de Kodamian passe son oblique bleue descendante
et vient buter sur sa résistance intermédiaire des 0.58€.(plus bas de novembre)
retour sur la Mm200 en vue ? suspens ! 
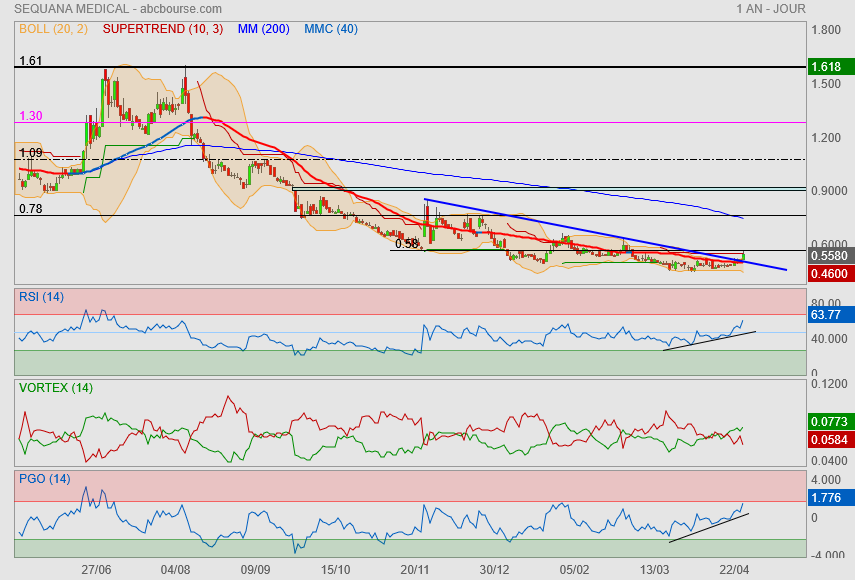
The annual results and annual report will be published on 28 April 2026.
Réponse obtenue par leur service relations avec les actionnaires.
Le calendrier est ainsi erroné sur la plupart des sites boursiers.
Juste à titre d'information pour ce titre dont ma performance avoisine les -77%.
Avec les résultats annuels ce mercredi, on en saura un peu plus sur les avancées aux Etats Unis .
Tentative de soulèvement
mais rattraper par mon oblique..
ce n'est que partie remise ! 
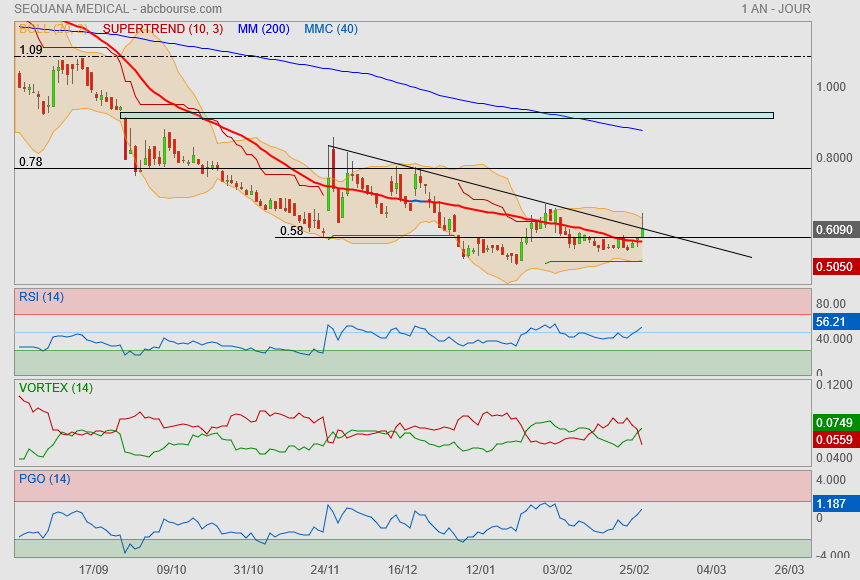
Raison de plus, c'est plus facile de couper en perte quand tout va bien pour le reste !
Tu vends un peu de plus value pour neutraliser ta perte et tu peux te faire une nouvelle ligne…
Y'a de bonnes occasions qui trainent…
Merci gars d'1.
Le portefeuille a pris 22,44% depuis le 01/01/2026, donc ça va
Je note : " l'action au ras des pâquerettes...."
C'est le principe même de lévitation d'une bouse plate …
: )
Je t'avais prévenu qu'il ne fallait pas rester sur cette bouse : tu es de plus plus loin de ton PRU et tu as perdu beaucoup de temps boursier avec l'argent que tu as mis dessus.
Même si c'est pas important, couper ses foyer de pertes et réinvestir ailleurs : ça assainit les comptes…
Concernant ce qui devrait arriver : les promesses n'engagent que ceux qui les croient et actuellement, même si elle faisait + 100%, tu serais encore loin de ton PRU…
; )
l'action au ras des pâquerettes....
cette année sera t elle celle de l'envolée ?
en tout cas, cette action a permis déjà de perdre 75% du capital investi ( pas plus que quelques euros à y mettre )
L'année 2026 marque une étape clé pour l'alfapump® aux États-Unis, avec la transition d'un lancement restreint vers un déploiement commercial complet ("Full Launch").
Voici les points essentiels concernant son implantation et sa disponibilité en 2026 :
1. Calendrier de déploiement en 2026
Lancement Complet (Q2 2026) : Après une phase de lancement initial ("Soft Launch"), Sequana Medical prévoit de débuter son déploiement à grande échelle au deuxième trimestre 2026.
Expansion des centres : La stratégie prévoit l'ajout d'environ cinq nouveaux centres d'implantation par trimestre à partir du lancement complet.
Objectif initial : La société visait la réalisation d'au moins 70 implantations commerciales dans huit centres de premier plan d'ici la fin du premier trimestre 2026.
2. Prise en charge financière (Remboursement)
Le système bénéficie d'un soutien financier renforcé pour faciliter son adoption en milieu hospitalier :
NTAP (New Technology Add-on Payment) : Depuis le 1er octobre 2025, l'alfapump bénéficie d'un paiement supplémentaire (jusqu'à 21 450 $) approuvé par les CMS (Centers for Medicare and Medicaid Services) pour l'exercice fiscal 2026.
Accessibilité : Ce codage spécifique aide les hôpitaux à couvrir les coûts du dispositif lors des procédures en milieu hospitalier.
3. La procédure d'implantation
L'implantation reste une intervention reconnue pour sa simplicité relative :
Technique : Procédure peu invasive d'environ 60 à 80 minutes, généralement réalisée par des radiologues interventionnels.
Dispositif : La pompe est placée sous la peau de l'abdomen avec deux cathéters : l'un recueillant le liquide d'ascite et l'autre le dirigeant vers la vessie pour une élimination naturelle par la miction.
Suivi : Le système est entièrement interne et se recharge sans fil à travers la peau.
Centres d'implantation notables (USA)
Plusieurs centres de renommée mondiale ont déjà commencé les implantations commerciales fin 2025, servant de base pour l'expansion de 2026 :
Mount Sinai Hospital (New York)
University of Pennsylvania (Philadelphie)
Mayo Clinic
Souhaitez-vous des détails sur les critères d'éligibilité pour les patients ou sur le fonctionnement de la recharge sans fil ?
Ces informations sont fournies à titre purement indicatif. Pour obtenir un diagnostic ou un avis médical, consultez un professionnel. Les réponses de l'IA peuvent contenir des erreurs. En savoir plus
Titre à surveiller !
Plus que jamais est au gout du jour...
40% potentiel à faire ==> gap + Mm200
ça se joue tant qu'on reste au dessus des 0.58€ 
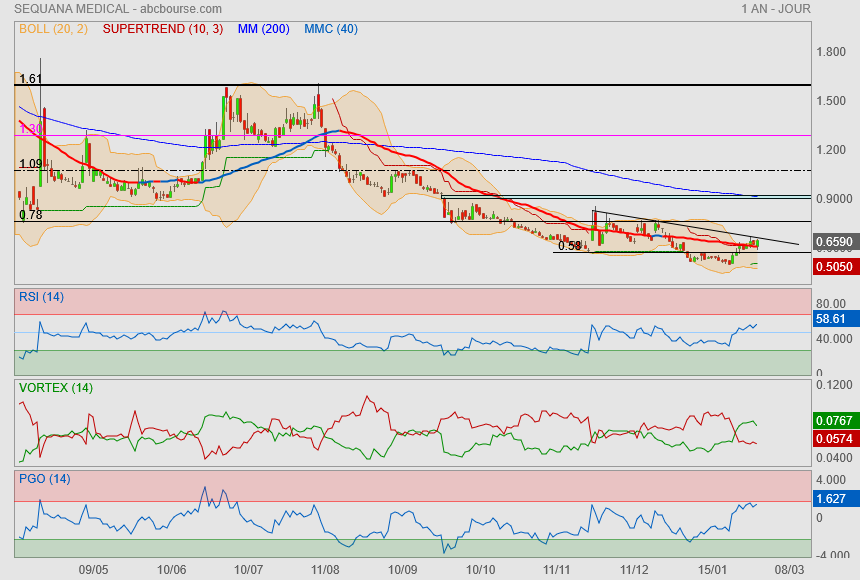
Reprise cette semaine (ça fait pas de mal vu la déconfiture)
mais le plus dur est encore devant nous.
Mm40 + Boll+ + supertrend + oblique
si ça passe, on ira sur le gap des 0.92€ et la Mm200 en prime 
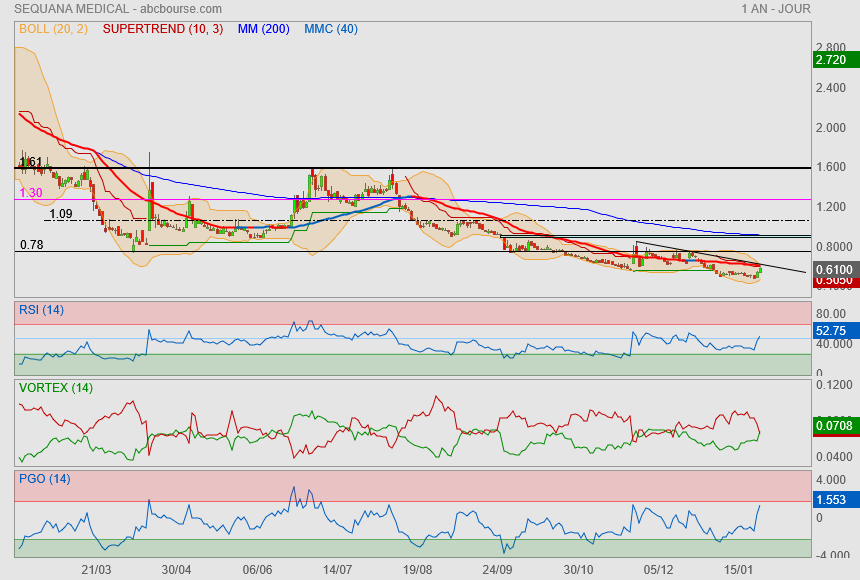
Sequana Medical N : annonce l'octroi d'un brevet américain supplémentaire important pour le DSR
Publié le 18-12-2025 à 09:39 - Modifié le 18-12-2025 à 10h06
• S’appuie sur des brevets DSR déjà accordés aux États-Unis, en Europe, au Japon et en Chine
• Renforce la protection des brevets de DSR grâce à une vaste expérience clinique et préclinique
• Les données publiées dans l’European Journal of Heart Failure confirment que la DSR représente une avancée majeure dans le traitement du syndrome cardiorénal et de l’insuffisance cardiaque résistante aux diurétiques.
• L’essai clinique américain MOJAVE comparant les diurétiques de l’anse administrés par voie intraveineuse à dose réduite (DSR) devrait entrer dans sa phase contrôlée randomisée après un financement dédié aux DSR.
Gand, Belgique – 18 décembre 2025 – Sequana Medical NV (Euronext Bruxelles : SEQUA, la « Société » ou « Sequana Medical ») , pionnière dans le traitement de la surcharge hydrique résistante aux médicaments dans les maladies hépatiques, l’insuffisance cardiaque et le cancer, a annoncé aujourd’hui l’obtention d’un brevet américain supplémentaire important pour son programme d’élimination directe du sodium (DSR). Le DSR est le programme de développement de médicaments de Sequana Medical pour le traitement du syndrome cardiorénal et de l’insuffisance cardiaque résistante aux diurétiques.
Le brevet américain n° 12 496 384 B2, intitulé « Formulations et méthodes d’élimination directe du sodium chez les patients atteints d’insuffisance cardiaque et/ou d’insuffisance rénale sévère », décrit la perfusion DSR et son fonctionnement. Plus précisément, il concerne l’administration intra-abdominale d’une perfusion sans sodium ou à faible teneur en sodium afin d’éliminer le sodium et, par conséquent, les fluides de l’organisme. Ce procédé permet de réduire la rétention d’eau chez les patients souffrant d’insuffisance cardiaque et présentant une fonction rénale résiduelle.
Ian Crosbie, directeur général de Sequana Medical, a déclaré : « Nous sommes ravis de l’obtention de ce brevet américain supplémentaire, qui, selon nous, renforce considérablement la protection de notre programme DSR. Ce brevet s’appuie sur notre vaste expérience préclinique et clinique avec le DSR, notamment les études RED DESERT et SAHARA, et consolide la protection de notre solution pour perfusion DSR de deuxième génération. Il s’agit de la formulation utilisée dans l’essai contrôlé randomisé américain MOJAVE, celle qui, nous en sommes convaincus, a le potentiel d’apporter des bénéfices cliniques significatifs aux cliniciens et aux patients, ainsi que des avantages commerciaux pour l’entreprise. Nous restons persuadés que le DSR représente une avancée majeure dans le traitement du syndrome cardiorénal et de l’insuffisance cardiaque résistante aux diurétiques, et nous avons hâte de reprendre l’essai MOJAVE dès la finalisation du financement dédié. »
@ gars d'1
l'année 2026 sera celle du début de la commercialisation d'alfapump aux états unis.
pour répondre à tes deux interrogations :
saches qu'il y a en partie une prise en charge par les assurances aux États Unis du traitement , dans la mesure où il constitue une économie par rapport au cout actuel des hospitalisations pour les patients souffrants d'ascite.
saches d'autre part que alfapump existe depuis plus d'une dizaine d'années et a fait ses preuves en Europe. On n'en est pas du tout aux phases d'essai thérapeutique et c'est pourquoi la FDA il y a un an à accorder l'autorisation de l'exploitation aux États Unis.
Le mieux je pense est que tu fasses un tour sur leur site internet pour essayer d'obtenir le maximum d'informations sur le produit.
Je comprends tout à fait tes interrogations mais celà justement doit inciter à la curiosité et à chercher peut être le plus d'éléments pour te faire une idée plus précise du produit .
Maintenant, il me semble avoir lu que le 20 décembre prochain, tu auras encore des actions qui seront émises par la société mais tu pourras trouver avec une petite recherche les modalités d'émission.
Ghent, Belgium, 5 December 2025 – Sequana Medical NV (Euronext Brussels: SEQUA) (the “Company” or “Sequana Medical“), a pioneer in the treatment of drug-resistant fluid overload in liver disease, heart failure and cancer, announces today a capital increase in the framework of (i) a contribution in kind of certain convertible receivables (for an aggregate amount of EUR 107,000.00) due under the convertible loan agreement entered into on 17 March 2025 between the Company and certain lenders (as amended), and (ii) a contribution in kind of certain convertible receivables (for an aggregate amount of EUR 1,500,000.00) due under the loan agreement entered into on 19 July 2022 between the Company and Kreos Capital VII (UK) Limited (as amended). As a result of aforementioned transactions, the Company’s share capital has increased on 5 December 2025 from EUR 7,054,460.23 to EUR 7,385,910.40 and the number of issued and outstanding shares has further increased from 68,089,899 to 71,289,225 ordinary shares, through the issuance of a total of 3,199,326 new shares. The applicable issue prices of the relevant new shares were determined in accordance with the terms of the relevant convertible loan agreements.
The total current number of outstanding subscription rights amounts to 7,476,821, which entitles their holders (if exercised) to subscribe to 8,643,549 new shares with voting rights in total, namely:
up to 261,895 new shares can be issued upon the exercise of 90,780 share options that are still outstanding under the ‘Executive Share Options’ plan for staff members and consultants of the Company, entitling the holder thereof to acquire ca. 2.88 new shares when exercising one of his or her share options (the “Executive Share Options“);
up to 681,779 new shares can be issued upon the exercise of 681,779 share options (each share option having the form of a subscription right) that are still outstanding under the ‘2018 Share Options’ plan for directors, employees and other staff members of the Company and its subsidiaries, entitling the holder thereof to acquire one new share when exercising one of his or her share options (the “2018 Share Options“);
up to 186,870 new shares can be issued upon the exercise of 186,870 share options (each share option having the form of a subscription right) that are still outstanding under the ‘2021 Share Options’ plan for directors, employees and other staff members of the Company and its subsidiaries, entitling the holder thereof to acquire one new share when exercising one of his or her share options (the “2021 Share Options“);
up to 994,750 new shares can be issued upon the exercise of 994,750 share options (each share option having the form of a subscription right) that are still outstanding under the ‘2023 Share Options’ plan for directors, employees and other staff members of the Company and its subsidiaries, entitling the holder thereof to acquire one new share when exercising one of his or her share options (the “2023 Share Options“);
up to 1,000,000 new shares can be issued upon the exercise of 1,000,000 share options (each share option having the form of a subscription right) that are still outstanding under the ‘2025 Share Options’ plan for directors, employees and other staff members of the Company and its subsidiaries, entitling the holder thereof to acquire one new share when exercising one of his or her share options (the “2025 Share Options“);
up to 302,804 new shares can be issued to Bootstrap Europe S.C.SP. upon the exercise of 10 warrants (each warrant having the form of a subscription right) that are still outstanding that have been issued by the extraordinary shareholders meeting of 27 May 2022 (the “Bootstrap Warrants“);
up to 1,567,819 new shares can be issued to Kreos Capital VII Aggregator SCSp. upon the exercise of 875,000 warrants (each warrant having the form of a subscription right) that are still outstanding that have been issued by the extraordinary shareholders meeting of 20 December 2024 (the “Kreos Warrants“)[1];
up to 1,057,632 new shares can be issued upon exercise of 1,057,632 subscription rights that are still outstanding that have been issued by the board of directors (within the framework of the authorized capital) on 27 April 2023 and 10 May 2023 in the framework of the private placement of new shares and new subscription rights (the “2023 Investor Warrants“); and
up to 2,590,000 new shares can be issued to GEM Global Yield LLC SCS (“GEM“) upon the exercise of 2,590,000 warrants (each warrant having the form of a subscription right) that are still outstanding that have been issued by the extraordinary shareholders meeting of 22 May 2025, entitling GEM to acquire one new share when exercising one of its warrants (the “GEM Warrants“).
Je note : "70.000 patients en attente de te trraitement "
A "30 000 $ ", le traitement, et vu la situation américaine en matière de santé, : y'en a combien qui peuvent se le payer ?
Ça sent le syndrome comptable Carmat à plein nez…
D'autant qu'on reste en phase d'essais cliniques, non : "Sequana annonce les premières implantations de l’alfapump en Pennsylvanie."
C'est pas interdit de rêver, mais faut aussi savoir être réaliste, non ?
Chasser outre mesure la bouse qui va décoller, sans avoir d'information précise concernant le créneau de décollage a rârement permis de faire fortune…
: )
Sequana annonce les premières implantations de l’alfapump en Pennsylvanie.
Selon un communiqué de presse de Sequana Medical (SEQUA), l’alfapump — la pompe qui évacue automatiquement le liquide vers la vessie en cas d’ascite due à une cirrhose du foie — commence progressivement à trouver sa place aux États-Unis.
L’Université de Pennsylvanie a réalisé ses premières implantations : deux patients ont reçu une alfapump le même jour.
Rappel
30.000 usd par intervention
70.000 patients en attente de te tresraitement
Des dizaines de centres seront prêts début 2026 pour pratiquer les interventions. Allez sur le site alfapump.com pour les informations.
Ces interventions font suite à une première implantation au Mount Sinai Hospital à New York. Sequana collabore désormais avec des Key Opinion Leaders dans d’importants centres médicaux afin de positionner l’alfapump comme le nouveau traitement de référence pour l’ascite réfractaire (accumulation de liquide dans la cavité abdominale) due à des maladies hépatiques sévères.
Message complété le 15/12/2025 08:26:55 par son auteur.
Les volumes sont à suivre durant les prochaines semaines pour voir s'il y a un regain d'intérêt pour la valeur.
Forum de discussion Sequana Medical
202604290454 1063500