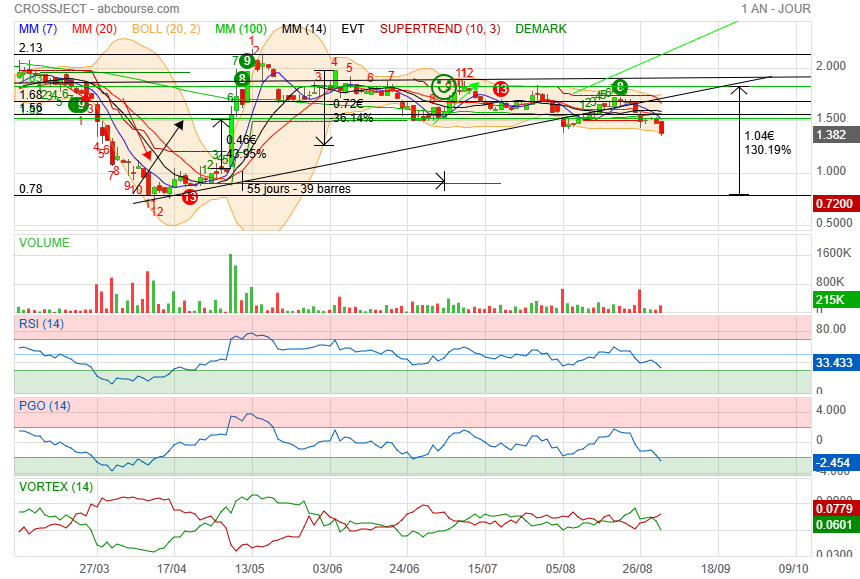
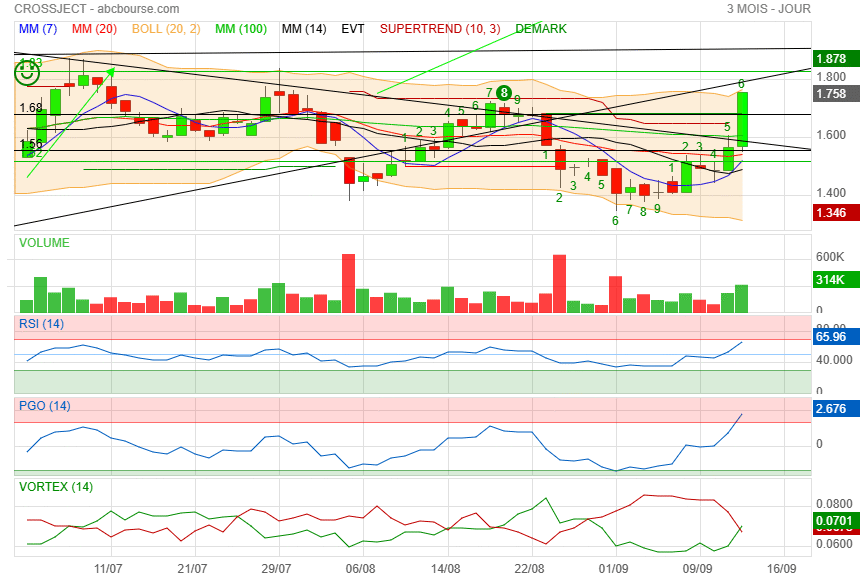
"Le pullback a été fait..
c'est maintenant que les acheteurs doivent sortir du bois "
------------------
Voili voilou 

Du volume en ce début de matinée .Possible passage des 2 euros ce jour.
Je note : " les acheteurs doivent sortir du bois"
Si c'est pour faire le feu sous la marmite, ça risque de devenir "rouge" !
: )
Le pullback a été fait..
c'est maintenant que les acheteurs doivent sortir du bois 

Communiqué de presse
CROSSJECT présente ses résultats financiers et les principaux faits marquants pour le premier semestre 2025
Position de trésorerie : 6.3 millions d'euros, contre 7,0 millions d’euros au 31 décembre 2024 montrant une très bonne maîtrise des ressources de la Société.
Investissements stables en R&D et augmentation de 3,1 millions d’euros des remboursements de R&D par BARDA1 pour le premier semestre 2024, à 6,5 millions d’euros, en lien avec la concentration des activités sur de développement réglementaire et les fabrications de lots liés à l’enregistrement de ZEPIZURE®.
La société a continué d’avancer vers le dépôt par BARDA de sa demande d'autorisation d'utilisation d'urgence (EUA) pour ZEPIZURE®.
Dijon, France, 24 septembre 2025, 22:00 CET -- CROSSJECT (ISIN: FR0011716265; Euronext: ALCJ), société pharmaceutique de spécialités qui développe des produits dédiés aux situations d’urgence fondés sur sa technologie propriétaire d’auto-injecteurs sans aiguille ZENEO®, annonce aujourd'hui ses résultats financiers pour le premier semestre clos le 30 juin 2025, et donne une mise à jour des faits marquants de son activité sur le premier semestre 2025.
Pendant cette période, CROSSJECT a poursuivi ses activités réglementaires conjointement avec la U.S. Biomedical Advanced Research and Development Authority (BARDA) visant à obtenir au plus tôt les autorisations réglementaires de ZEPIZURE® aux Etats-Unis.
Dans ce contexte, en juin, et comme annoncé en mai 2025, CROSSJECT et son partenaire CDMO EUROFINS, ont produit les lots de validation dont les données font partie du dossier EUA et organisé la fabrication de lots afin qu’ils soient disponibles au moment de l’évaluation de l’EUA,
Au-delà de la période de référence au 30 juin 2025, CROSSJECT continue ses activités liées à l’enregistrement de ZEPIZURE®, en particulier :
La société et BARDA ont utilisé la période estivale pour la rédaction et la revue détaillée du dossier.
BARDA a conduit en septembre des audits à blanc destinés à préparer la société à de potentielles inspections de la FDA.
Par ailleurs, la Société a obtenu en septembre une extension du financement R&D de 11,3 millions d’euros dans le cadre de son contrat avec le Gouvernement Américain.
D’autres éléments marquants sont également intervenus post clôture :
La société a obtenu une nouvelle ligne de crédit de 750,000 euros d’un nouveau partenaire bancaire ;
La société a obtenu le renouvellement de sa certification ISO 13485 pour l’ensemble de ses sites (Dijon et Gray) ;
La société a également vu son certificat de Bonnes Pratiques de Fabrication (GMP) prolongé.
Dans le contexte macro-économique actuel, la société et ses conseils estiment aujourd’hui ne pas être exposée à un impact lié aux augmentations de droits de douane de l’Europe vers les Etats-Unis sur les livraisons destinées à la BARDA ;
Nous rappelons par ailleurs, qu’en préparation de l’augmentation de ses volumes de production lors de la commercialisation de son portefeuille de produits, la société a finalisé pendant ce premier semestre le développement et l’introduction de son module ZENEO® Nest, dernière innovation de la ZENEO® Factory. Le ZENEO® Nest facilite et accélère les opérations de remplissage aseptique sur des lignes automatisées à haute cadence disponibles chez de nombreux CDMO.
Enfin dans le cadre de sa stratégie de commercialisation directe aux États-Unis la Société a continué à renforcer le potentiel de ZEPIZURE® en collaboration avec des leaders d’opinion en épilepsie et en médecine d’urgence.
« Tout au long de 2025, CROSSJECT a continué de progresser de façon décisive vers le dépôt de dossier EUA de ZEPIZURE®. Nous exprimons notre gratitude à la BARDA pour sa diligence et sa consistance dans la revue des données et son attention portée à notre outil de fabrication. Pragmatique, et désireuse de sécuriser l’enregistrement de ZEPIZURE® dans les meilleurs délais, la BARDA nous a aussi gratifié d’une augmentation majeure (de plus de 11 millions de dollars) de sa contribution. », a déclaré Patrick ALEXANDRE, Président du Directoire de CROSSJECT.
Voir également les annexes 1 (compte de résultat), 2 (bilan actif) et 3 (bilan passif).
1 Contrat n° 75A50122C00031 avec le ministère de la santé et des services sociaux ; administration pour la préparation et la réponse stratégiques ; autorité pour la recherche et le développement biomédicaux.
Bonjour a tous
Effectivement je pariai aussi sur une hausse suite a la nouvelle j ai même repris quelques titres !

Les nouvelles sont bonnes mais ne font pas remonter le cours pour autant !
🧐🔎👀☹️
CROSSJECT obtient un financement supplémentaire de la BARDA pour soutenir le développement et l'autorisation par la FDA de ZEPIZURE®
Publié le 22/09/2025 à 07:30
DIJON, France – 22 septembre 2025 (07H30 CET) – CROSSJECT (ISIN : FR0011716265 ; Euronext : ALCJ), société pharmaceutique internationale spécialisée dans le développement d'auto-injecteurs sans aiguille pour les situations d'urgence, confirme aujourd'hui l'octroi d'un financement supplémentaire de 11,3 millions de dollars par la Biomedical Advanced Research and Development Authority (BARDA) américaine. Cela porte à 43,3 millions de dollars le financement total du contrat pour le développement du ZEPIZURE®. Ces nouveaux fonds soutiennent les activités réglementaires et de fabrication qui ont progressé en termes de précision au cours du processus de développement en vue de l'obtention des autorisations d'utilisation d'urgence (EUA) et de mise sur le marché (NDA) par la FDA.
CROSSJECT et la BARDA continuent de réaliser des progrès importants en vue de satisfaire aux exigences réglementaires pour les demandes d'EUA et de NDA prévues prochainement. Parmi les avancées récentes notables, la société met en avant la fabrication de plusieurs lots de validation conformes et la réalisation d'un audit des installations.
Comme annoncé précédemment, dès l'obtention de l'autorisation de la FDA, l'acquisition contractuelle de 306 000 auto-injecteurs ZENEO® Midazolam pour adultes et de 54 000 auto-injecteurs ZENEO® Midazolam pour enfants, pour un montant total de 60 840 000 dollars, sera réalisée.
Patrick ALEXANDRE, Président du Directoire, a déclaré : « Nous sommes reconnaissants à la BARDA pour son partenariat et son investissement continus, qui soulignent l'importance de ZEPIZURE® pour le programme CHEMPACK et l'initiative américaine Strategic National Stockpile. Nous abordons avec confiance les étapes clés de la réglementation et de la production commerciale, grâce au travail assidu de nos équipes internes, de nos partenaires de fabrication et à la force de notre collaboration avec la BARDA. »
Super nouvelle !!! 👍
Message complété le 18/09/2025 11:41:37 par son auteur.
Le PDG, Patrick Alexandre, aurait créé une Société par Actions Simplifiée Unipersonnelle le 21 juillet 2025 dénommée IKATEQ (siège social à Gray) et enregistrée au greffe de Vesoul le 6 août 2025. Activité principale déclarée: "activité des sièges sociaux".
Tout est en ligne sur divers sites d'informations légales.
Interprétation/hypothèse:
La SASU d'après de nombreux sites est un outil d'optimisation fiscale et sociale. Genre holding? Étant donné la date de création, peu de temps avant des annonces attendues, on peut considérer que c'est un signe avant-coureur positif. C'est bien qu'il attend quelque chose!
https://www.fpds.gov/ezsearch/search.do?indexName=awardfull&templ ateName=1.5.3&s=FPDS.GOV&q=crossject
Rallonge de la BARDA à priori de $11,291,005.00
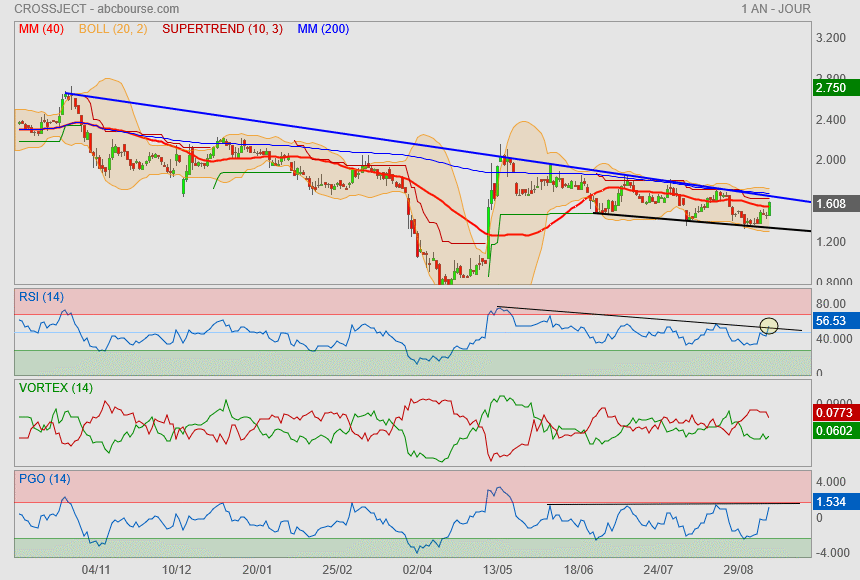
Tiens une bougie au dessus de l'oblique et de la Mm200..
va t'elle tenir sur la journée cette fois ?

Blocage Mm200
ça rigole pas niveau indicateurs 
PS : je poste pour essayer d'effacer la malédiction Philiberts. hihi
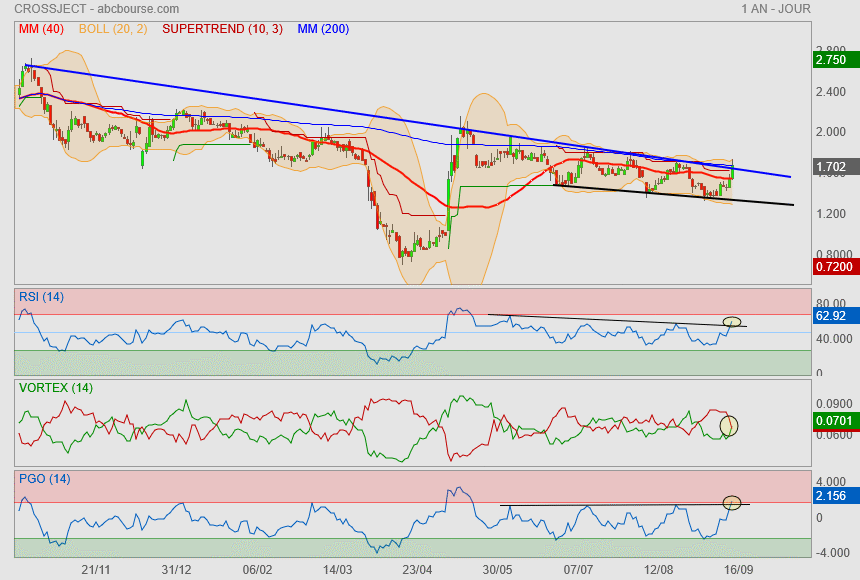
bien orchestré on fait monter la mayonnaise à la limite de RH et on balance 30000 titres
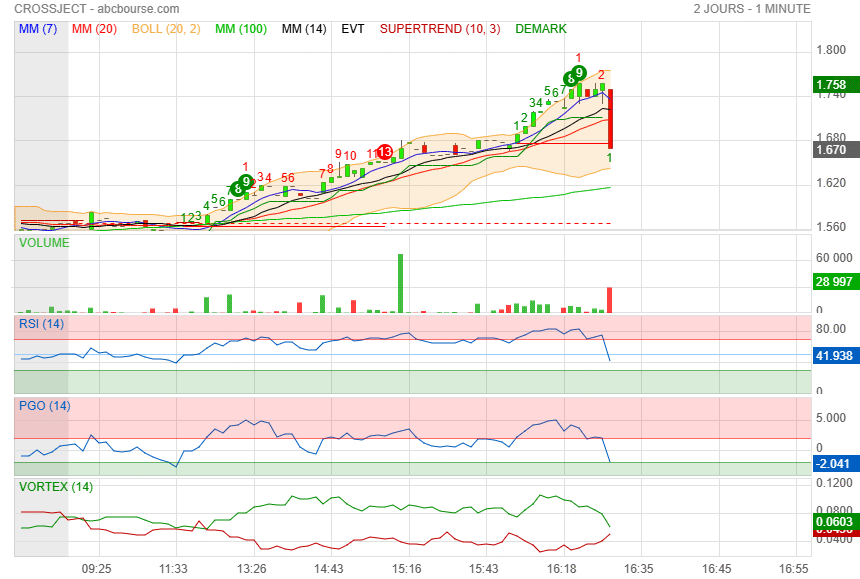
Je vais poster avant que Philiberts lui fasse peur...
encore u essai de pétage d'oblique cumulée au supertrend et surtout à la Mm200 
Euronext fait connaître que 423.560 actions nouvelles émises par CROSSJECT, immédiatement assimilables aux actions existantes, seront admises sur EURONEXT GROWTH PARIS à partir du 02/09/2025.
👀🔎👀🔎👀
Effectivement c est le cas me suis allégé ! j essaye de sortir ces prochains jours au mieux sur plusieurs valeurs