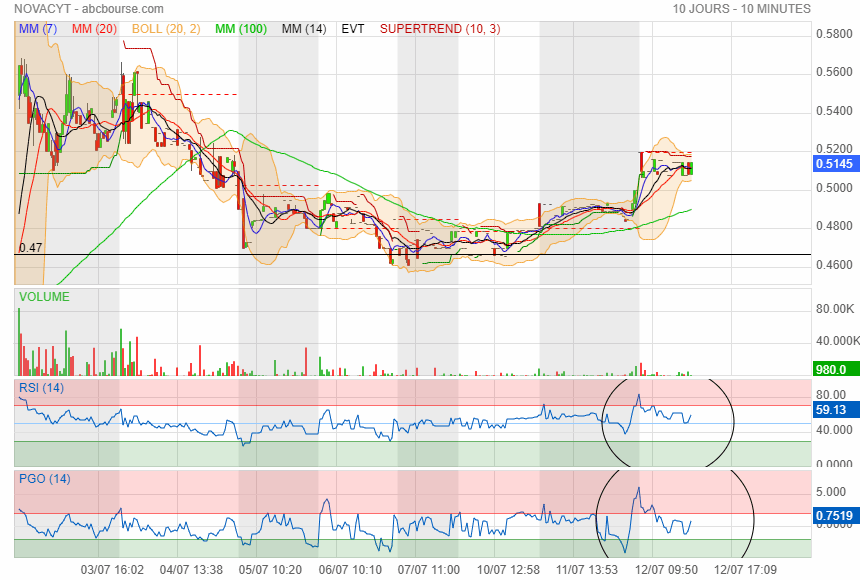
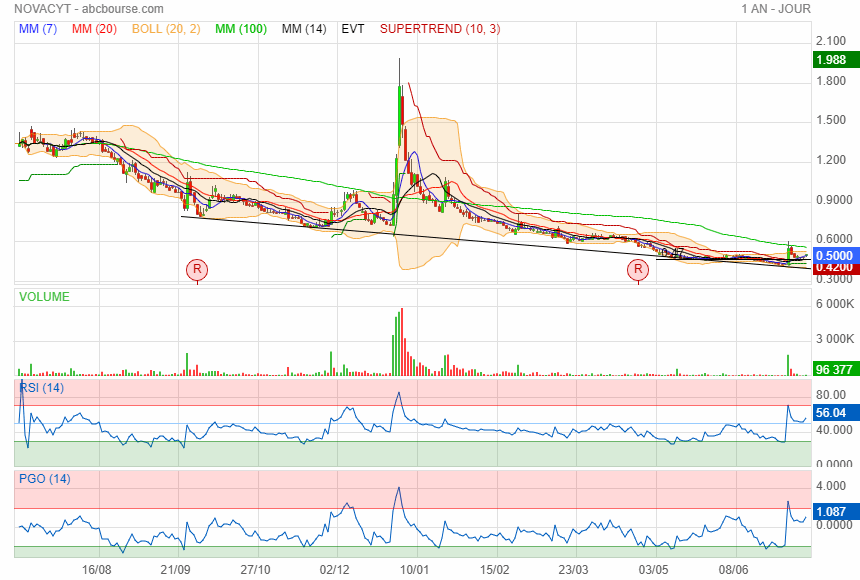
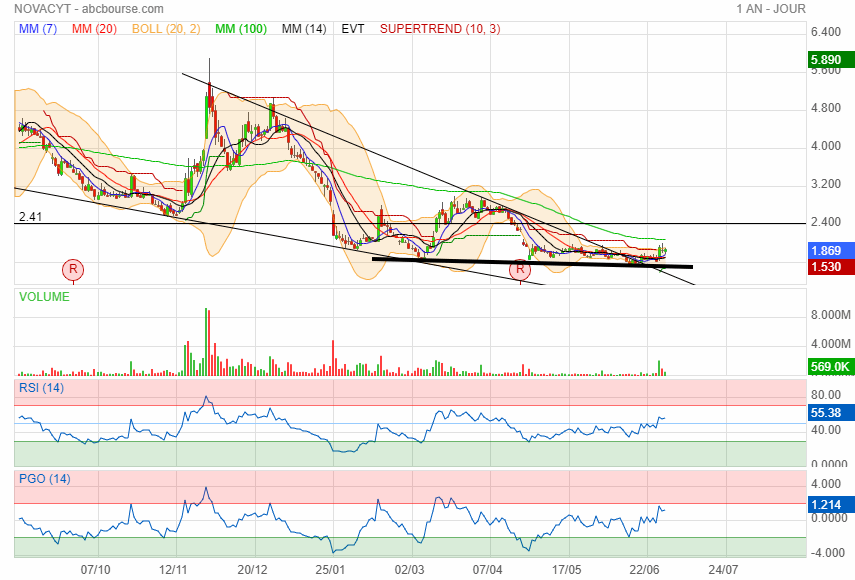
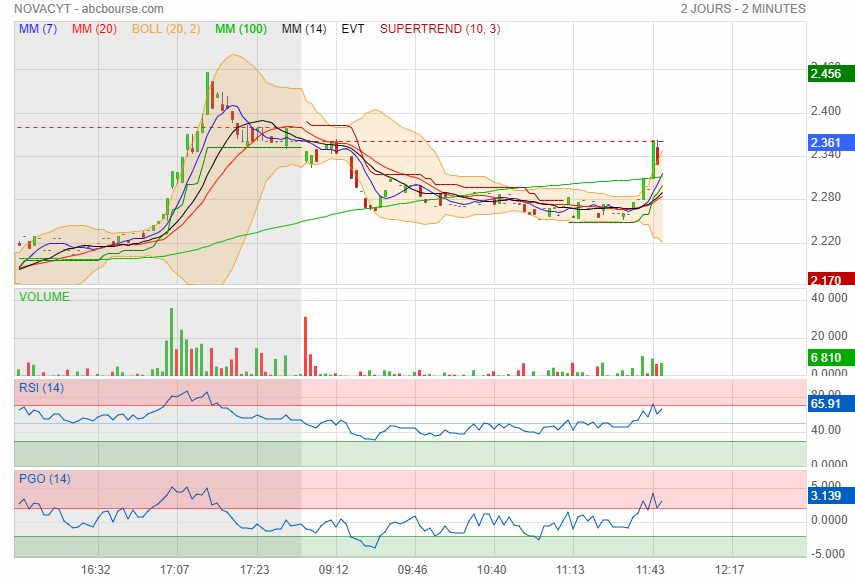
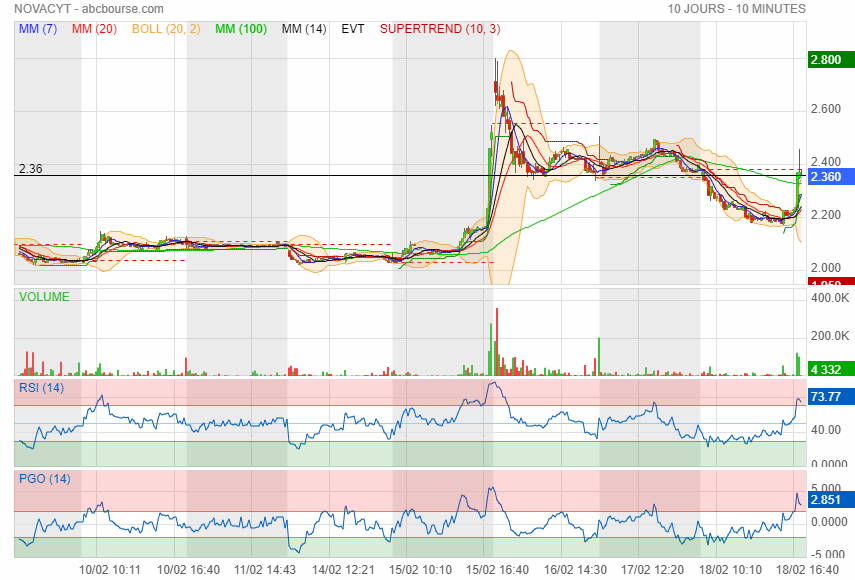
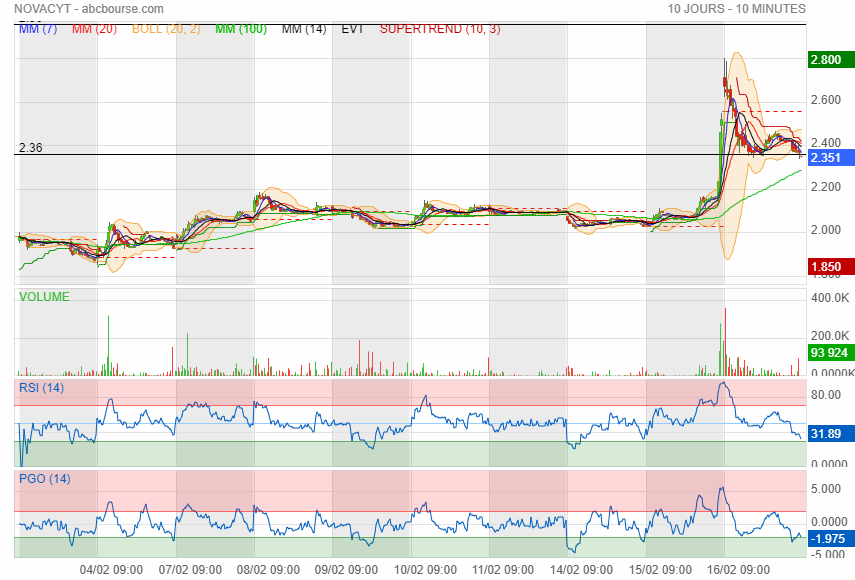
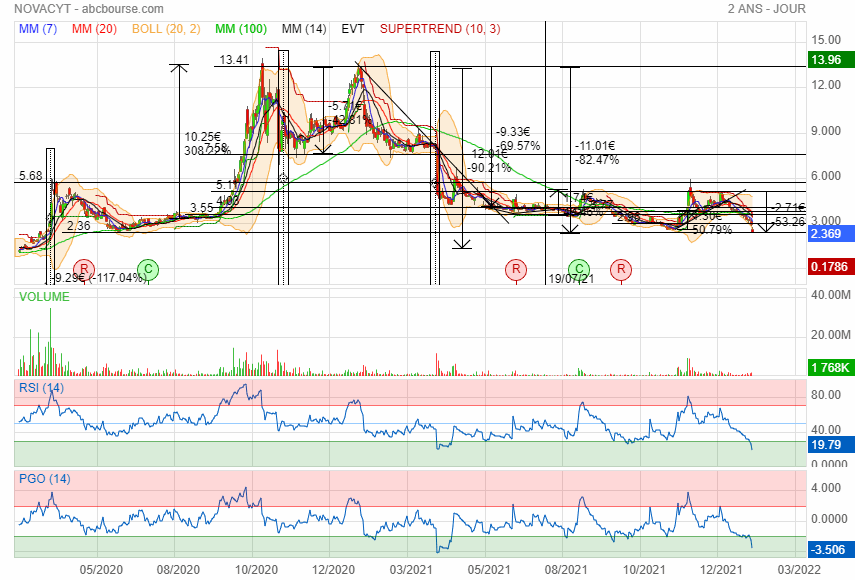
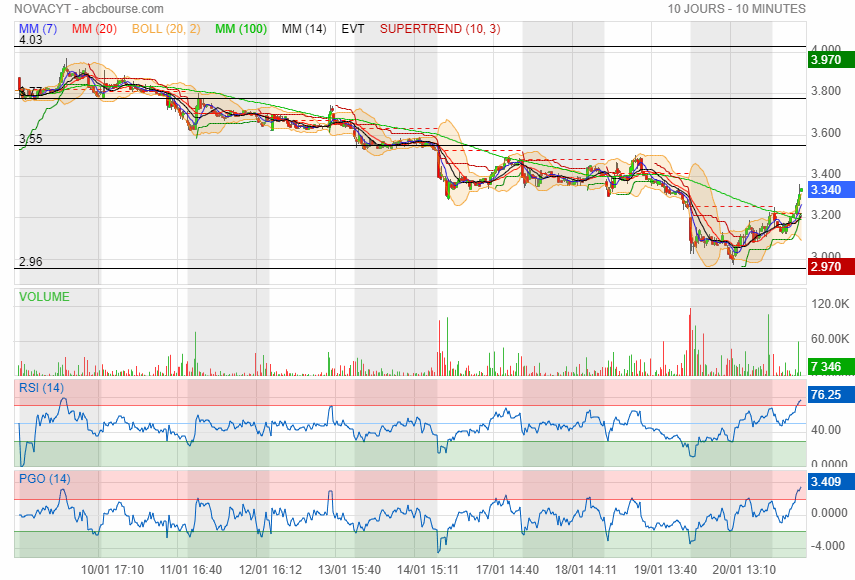
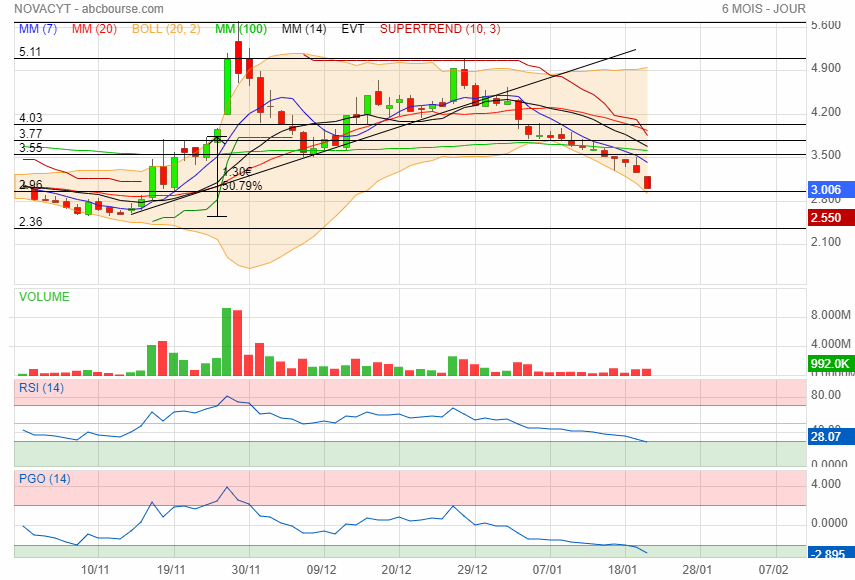
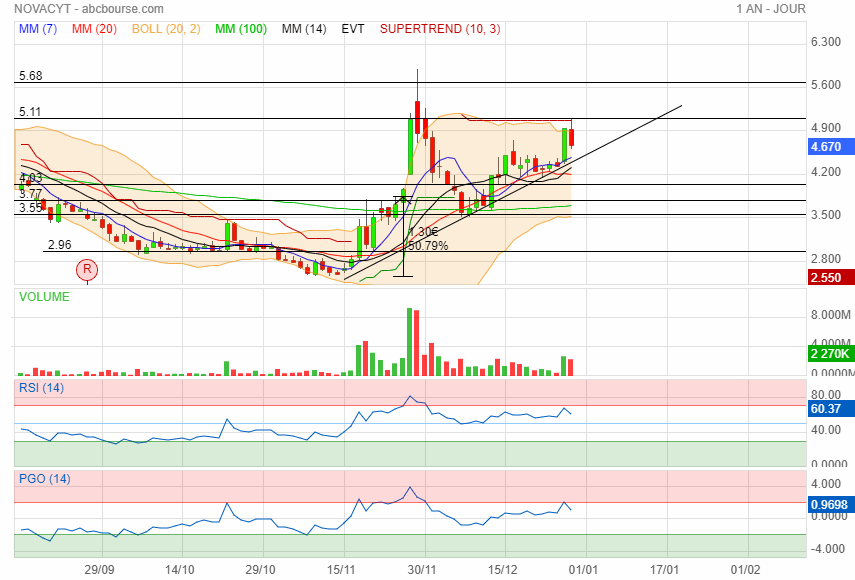
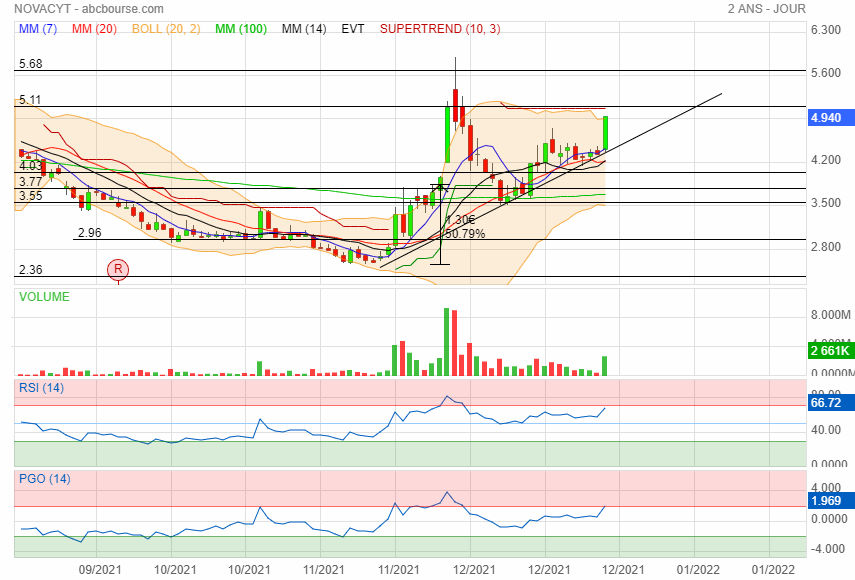
changement de tendance à la hausse ca va faire 3 ans qua elle baisse
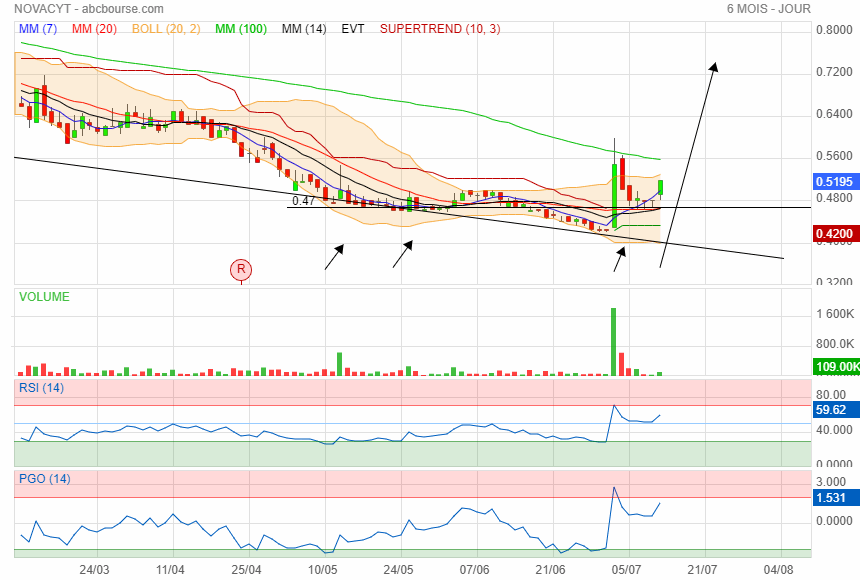
Vous avez raison Philibert,
A part attendre une épidémie mondiale de la variole du singe, je ne vois pas... désolé
Tonio votre remarque n est pas productive ou alors merci de m'éclairer sur la stratégie sur novacyt
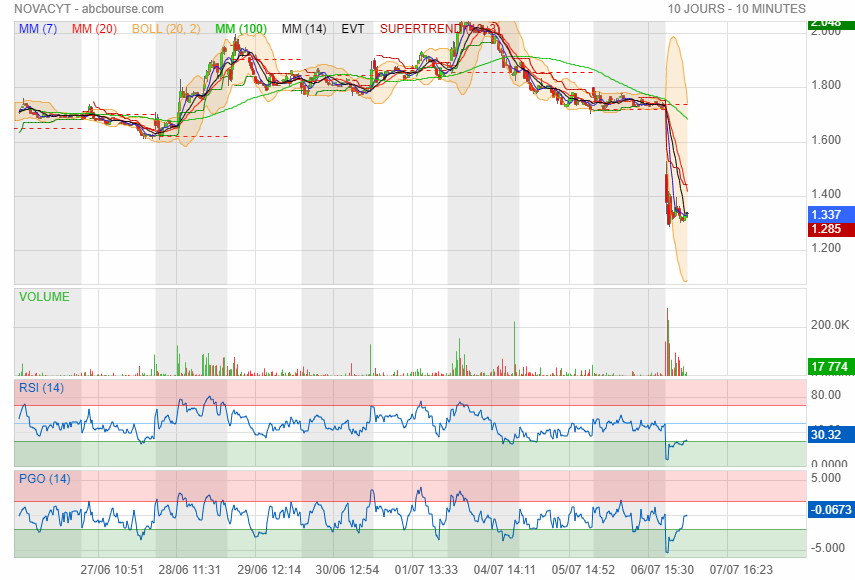
Non c'était pas le bon moment
mais bon je peux que m en vouloir j aurai du sentir le coup fourré suite aux ventes précipités depuis deux trois jours
Au 14février 2022, la participation de Biosynex dans la Société sur la base du vote et du capital est de 4,04% (2 855 959 actions).
Novacyt : Participation dans la Société
Communiqué de presse [PDF] • 18/02/2022 | 17:22
https://live.euronext.com/sites/default/files/Connect_novacyt-biosynex-holdings-18022022-french.pdf
Paris, France et Camberley, Royaume-Uni - 18 février 2022 -
Novacyt (EURONEXT GROWTH : ALNOV ; AIM : NCYT), spécialiste international du diagnostic clinique, annonce que Biosynex SA ("Biosynex") lui a notifié le 18 février 2022 qu'au 14 février 2022, la participation de Biosynex dans la Société sur la base du vote et du capital est de 4,04% (2 855 959 actions).
Pour de plus amples renseignements, veuillez consulter le site www.novacyt.com ou contacter : Novacyt SA David Allmond, Chief Executive Officer James McCarthy, Chief Financial Officer +44 (0)1276 600081 SP Angel Corporate Finance LLP (Nominated Adviser and Broker) Matthew Johnson / Charlie Bouverat (Corporate Finance) Vadim Alexandre / Rob Rees (Corporate Broking) +44 (0)20 3470 0470 Numis Securities Limited (Joint Broker) Freddie Barnfield / James Black +44 (0)20 7260 1000 Allegra Finance (French Listing Sponsor) Rémi Durgetto / Yannick Petit +33 (1) 42 22 10 10 [email protected]/ [email protected] FTI Consulting (International) Victoria Foster Mitchell / Alex Shaw +44 (0)20 3727 1000 [email protected] / [email protected] FTI Consulting (France) Arnaud de Cheffontaines FTI Consulting +33 (0)147 03 69 48 [email protected]
A propos de Novacyt Group
Le Groupe Novacyt est une entreprise internationale de diagnostic qui génère un portefeuille croissant de tests de diagnostic in vitro et moléculaire. Ses principales forces résident dans le développement de produits de diagnostic, la commercialisation, le développement et la fabrication pour tiers. Les principales unités commerciales de la Société comprennent Primerdesign et Lab21 Products, qui fournissent une vaste gamme de tests et de réactifs de haute qualité dans le monde entier. Le Groupe sert directement les marchés de la microbiologie, de l'hématologie et de la sérologie ainsi que ses partenaires mondiaux, dont les grands acteurs du secteur. Pour plus d'informations, veuillez consulter le site Internet : www.novacyt.com
Aujourd'hui c'est la pêche au chalut(*) de grand fond pour racler les crevettes, sauf pour novacyt...
on recommence
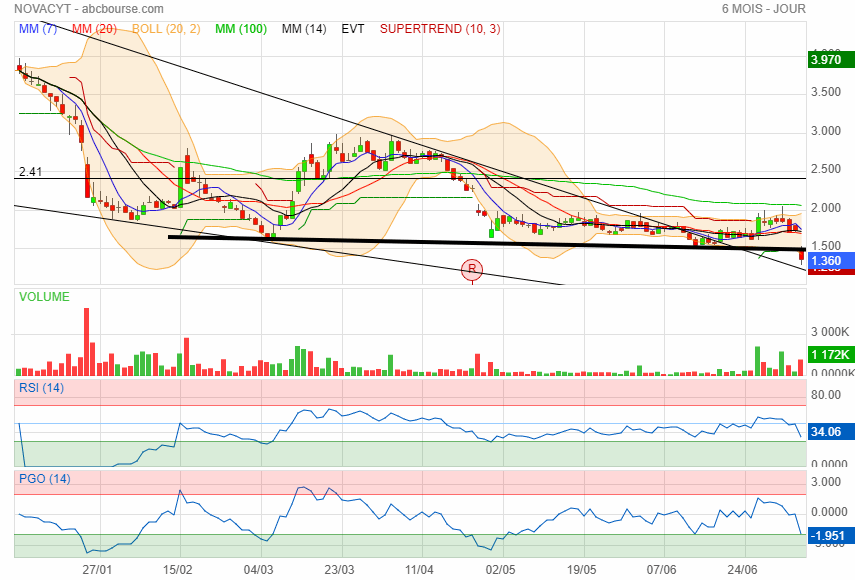
Résistance 5.11
Avec les bruits qui courent ca devrait passer
Journée d enfer pour les actions covid allez voir la clôture de theradiag