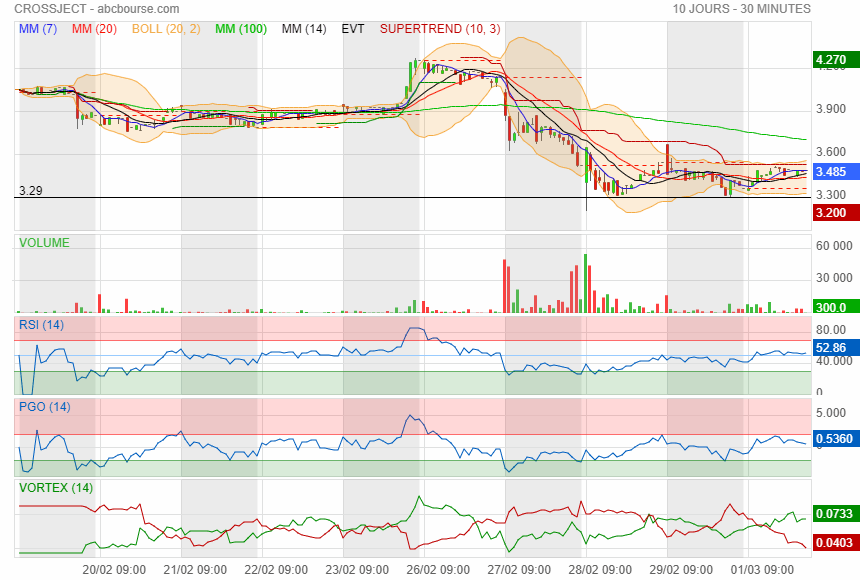
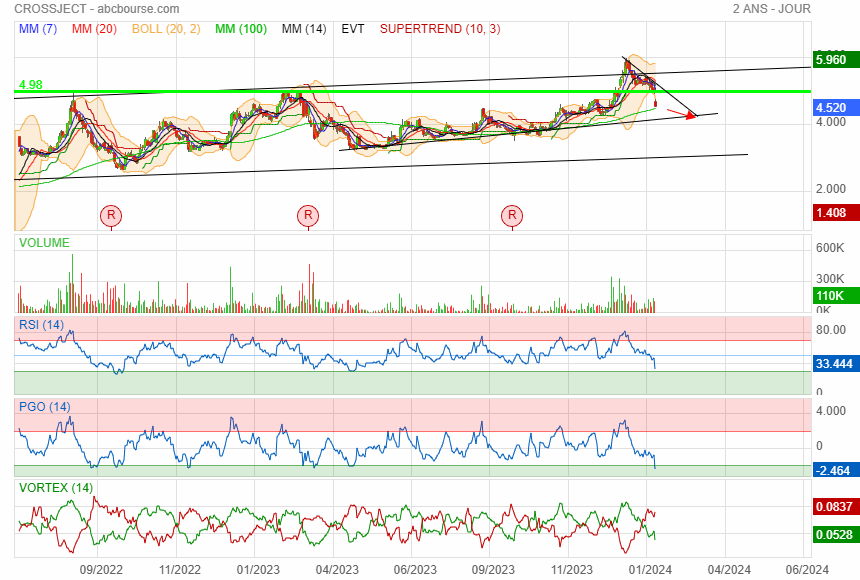
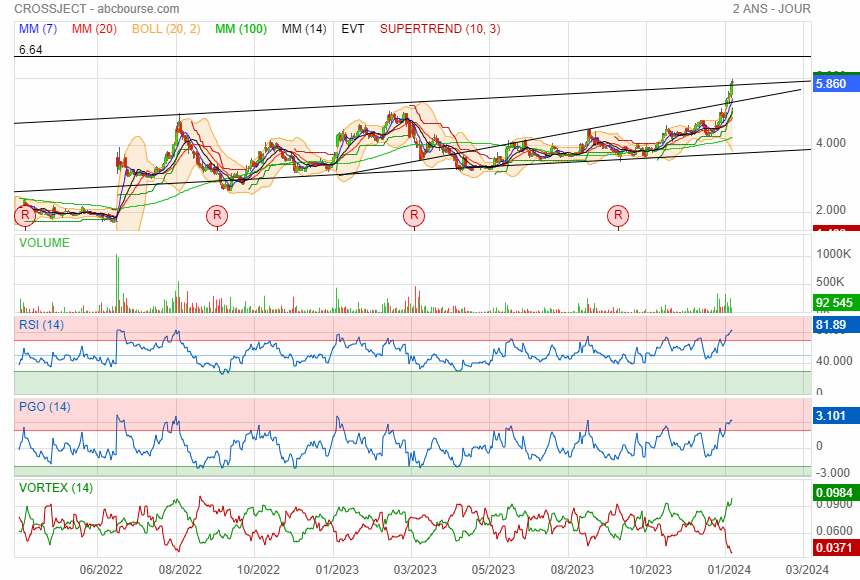
Douche froide
effectivement la ces plus des rumeurs
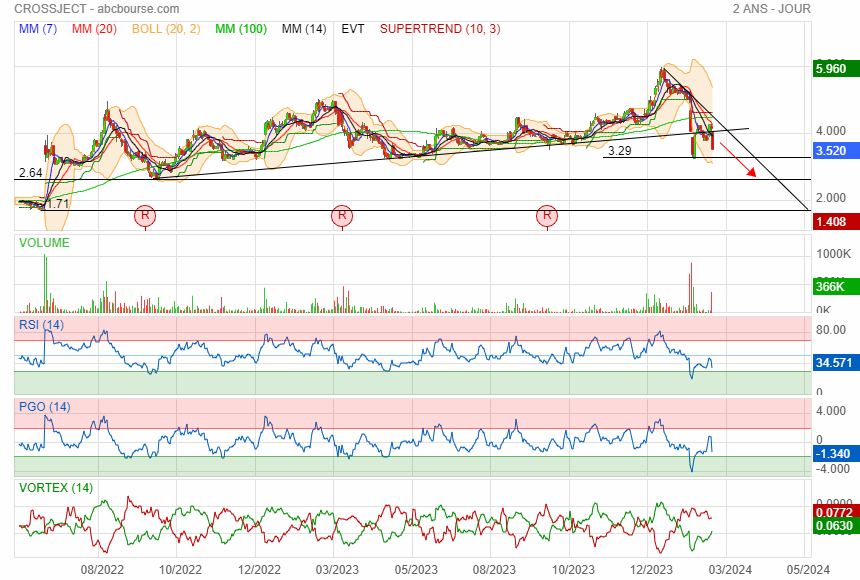
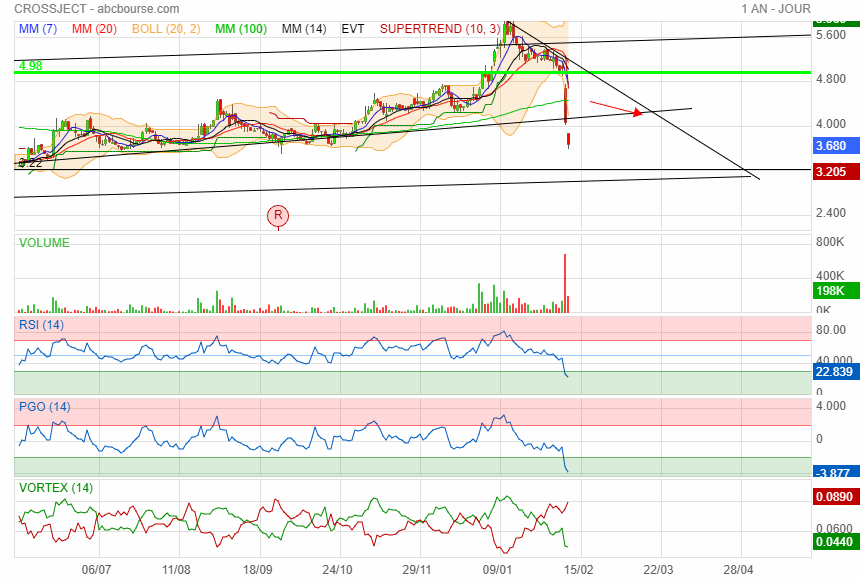
premier support à 3.29 puis 2.64
et puis ensuite direction le gap
on en est pas encore la
(Boursier.com) — Crossject annonce l'émission, avec suppression du droit préférentiel de souscription au profit d'une catégorie de personnes, de 70 Obligations Convertibles en Actions Nouvelles et Amortissables (OCAs) d'une valeur nominale de 100.000 euros chacune, et pour un montant brut de 7 millions d'euros, conformément à la 13ème résolution de l'assemblée générale mixte du 7 juin 2023 et à la décision prise le 26 février 2024 par un membre du Directoire agissant dans le cadre de la subdélégation consentie par le Directoire lors de sa réunion en date du 23 février 2024 sur autorisation du Conseil de Surveillance en date du 29 janvier 2024. "Nous sommes fiers de réunir ces nouvelles ressources financières auprès d'une entité gérée par Heights Capital Management, Inc., investisseur institutionnel spécialisé dans le financement des sociétés en croissance, qui est un gage de confiance dans nos avancées industrielles et commerciales, en particulier sur le continent nord-américain", ajoute Patrick Alexandre, Président du Directoire.
Ces fonds s'ajoutent au financement actuel par la BARDA (dont 6,7 M$ facturés sur 2023 sur un budget global maximal de 32 M$), dans le cadre du contrat 75A50122C00031, pour le développement avancé de l'auto-injecteur ZENEO-midazolam (nom proposé ZEPIZURE) par approbation de la Food and Drug Administration des États-Unis pour la prise en charge de l'état de mal épileptique. Le contrat comprend également de futures perspectives pour la fourniture pour 60 M$ de ZEPIZURE, qui seront livrés au gouvernement américain, une fois le produit autorisé par la FDA pour utilisation d'urgence... La forme prise par le financement accordé par Heights "répond à notre objectif prioritaire d'avoir des solutions avec remboursement en numéraire au fil de l'eau et une dilution limitée", ajoute Patrick Alexandre.
Ce financement maximum de 12 ME vient s'ajouter aux autres financements non-dilutifs récemment sécurisés (opération de cession-bail immobilière pour environ 5 ME, préfinancement du Crédit Impôt Recherche 2023 pour 1,5 ME sur un total de de 3 ME, etc.) et aux revenus commerciaux liés aux partenariats nouveaux ou existants.
Le financement de Heights peut aller jusqu'à 12 millions d'euros et est composé de 2 tranches : une première tranche de financement de 7 millions d'euros pouvant être complété par une seconde tranche d'un montant maximum de 5 millions d'euros, à l'initiative de Crossject et sous réserve de la satisfaction de certaines conditions préalables.
COTATION
La Première Tranche passe par l'émission, avec suppression du droit préférentiel de souscription dans le cadre d'une catégorie de personnes telle que définie par l'assemblée générale du 7 juin 2023 au bénéfice de Heights, de 70 OCAs d'une valeur nominale de 100.000 euros chacune, la souscription par l'investisseur des 70 OCAs à hauteur de 90% de leur valeur nominale soit 6,3 millions d'euros (90.000 euros par OCA), et un règlement-livraison le 28 février 2024, sous réserve de la satisfaction de conditions usuelles. Le nombre d'actions nouvelles pouvant être émises au titre des OCAs sera compris entre 1.359.434 et 7.816.666 - 1.359.434 actions maximum en cas de conversion de la totalité des 70 OCAs au prix de conversion de 5,1492 euros fixé à 135% du prix de référence initial de 3,8142 euros (lequel est susceptible d'ajustements), ou, 2.383.420 actions maximum, en cas d'option par la société pour un amortissement en actions nouvelles des 70 OCAs (au prix plancher actuel de 3,2796 euros et dans la limite de détention de 9,99% du capital de la Société par l'Investisseur), ou 7.816.666 actions maximum, en cas d'option par la société pour un amortissement en actions nouvelles de tout ou partie des 70 OCAs (au nouveau prix plancher de 1 euro et dans la limite de détention de 9,99% du capital de la Société par l'investisseur).
Concernant la Seconde Tranche, le groupe indique que durant une période de douze mois à compter du 28 juin 2024 (soit à compter de la date de première échéance de remboursement de la Tranche 1 des OCAs), Crossject aura le droit (et non l'obligation) de solliciter le tirage total ou partiel de la Seconde Tranche dès lors que les conditions cumulatives suivantes seront satisfaites :
- Une AGE doit avoir approuvé l'émission de la Seconde Tranche des OCAs ;
- Crossject doit avoir reçu l'autorisation de la US Food and Drug Administration (FDA) afin de livrer les premières unités de ZEPIZURE au Strategic National Stockpile relatives au contrat entre Crossject et la BARDA ; et
- Le montant total en principal des OCAs émises au titre de la Seconde Tranche ne doit pas dépasser 10% de la capitalisation boursière de Crossject à la date à laquelle les conditions 1 et 2 sont satisfaites.
Elle a refermer le 1 ier gap plus vite que prévue
Vient de repasser au-dessus de l'oblique !
A suivre
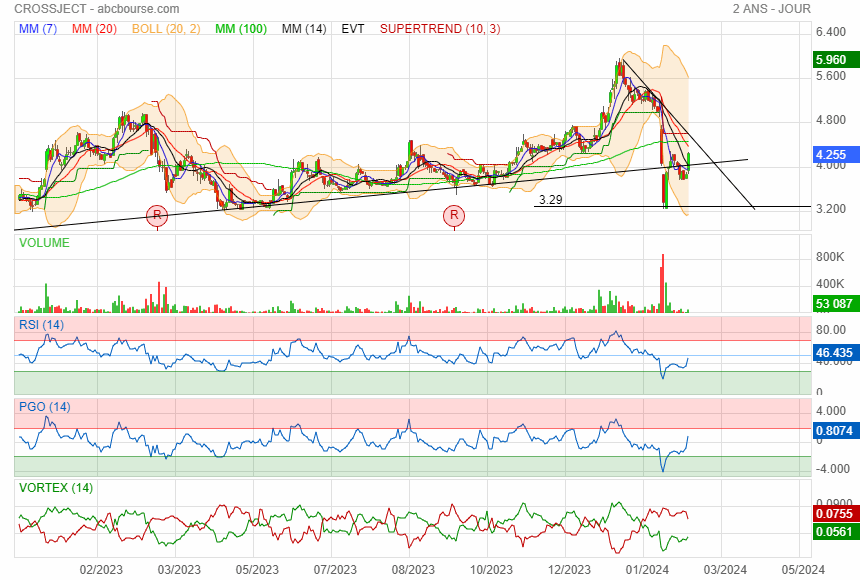
le rebond a eu lieu avec du volume
perso je pense pas qu elle referme le gap 3.90 risque de devenir résistance on verra ces prochains jours
j ai presque tout revendu sur 3,84 acht sur 3.31
J ai bien limité la casse
maintenant j'attend de voir
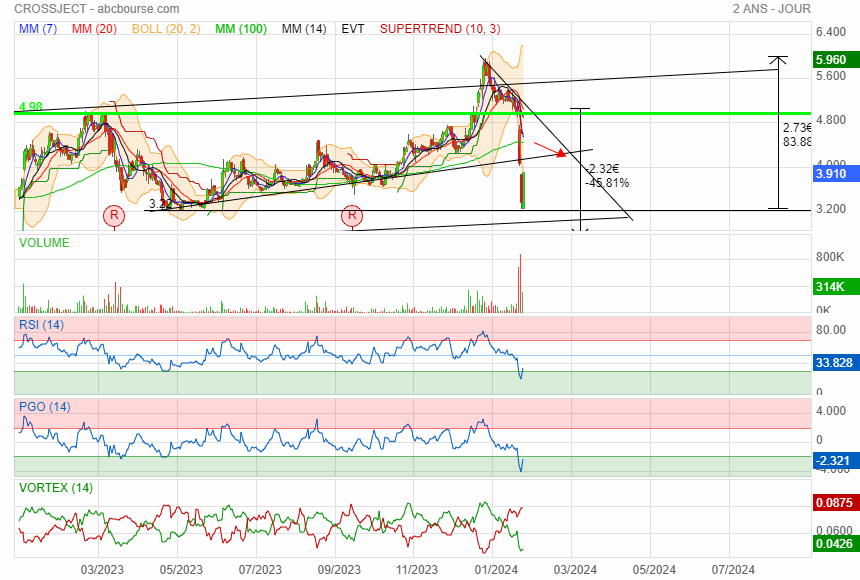
Dans l état actuel 1.80 sur une rumeur d Ak ca n'a pas de sens
Faire moins de 37% en 2 jours c est déjà pas mal
on va déjà voir comment elle réagit sur le support oblique vers 2.95 si elle descend si bas .
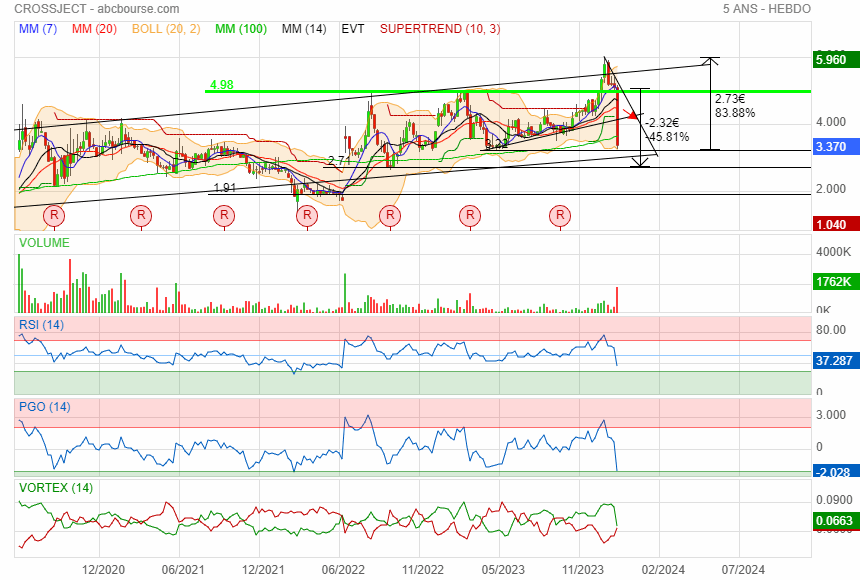
CROSSJECT : Pas de nouvelles? Pas forcément une bonne nouvelle
Le 08 février 2024
STRATEGIC PLAN
La présentation de mardi dernier ne nous a pas vraiment renseignés (voire pas du tout) sur le développement du groupe sur la période récente. Nous regrettons qu’aucune nouvelle précision n’ait été donnée concernant les procédures de dépôt aux États-Unis (Emergency Use Authorization), en particulier en termes de calendrier. Nous déplorons également qu’il faille attendre aussi longtemps (soit jusqu’à fin avril !) pour avoir un aperçu sur les comptes annuels 2023 et les perspectives financières compte tenu des nouveaux besoins en matière de financement. En résumé, nous sommes déçus.
ACTUALITÉ
Le groupe a organisé un webcast le 6 février pour faire le point sur son développement sur la période récente et sa stratégie commerciale pour 2024.
ANALYSE
Pour commencer et pour être francs, nous avons trouvé la présentation plutôt “creuse”, commençant par un rappel de ce que propose Crossject, soit le(s) produit(s) qu’elle entend vendre et les progrès réalisés ces vingt dernières années.
Le groupe a rappelé qu’il avait conclu un accord aux Etats-Unis avec Syneos, un prestataire de services, qui devrait l’aider à déposer ses dossiers réglementaires aux États-Unis et à lancer commercialement son produit ZENEO une fois les autorisations accordées. En outre, le groupe a de nouveau confirmé poursuivre ses efforts pour faire approuver et commercialiser son ZEPIZURE (au travers notamment d’un accord de licence avec AFT Pharmaceuticals pour l’Australie et la Nouvelle-Zélande et d’un nouvel accord de commercialisation pour l’Europe du Nord). Il a ensuite réaffirmé son intention de se concentrer en 2024 sur les approbations réglementaires pour ZEPIZURE. Si l’ensemble de ces points vont dans le bon sens, ils ne sont pas nouveaux.
En janvier 2024, Crossject a engagé Syneos Health, groupe de services aux laboratoires biopharmaceutiques totalement intégré, pour la préparation au lancement commercial aux États-Unis de son auto-injecteur ZENEO-midazolam (nom proposé ZEPIZURE), un traitement d’urgence innovant dans la prise en charge des crises d’épilepsie y compris celles causées par l’exposition à un agent neurotoxique. Fortement implanté aux Etats-Unis, Syneos Health apportera une réelle expertise dans la commercialisation de nouvelles thérapies à Crossject, au moment même où ce dernier s’apprête à déposer une demande d’autorisation de mise sur le marché. Les principaux détails du contrat signé avec la BARDA aux États-Unis ont également été rappelés (cf. nos précédents commentaires sur le sujet).
Selon le groupe, les discussions avec la FDA concernant les exigences nécessaires à l’autorisation d’utilisation d’urgence de ZEPIZURE sont “en bonne voie”. Si nous ne doutons pas de sa véracité, cette déclaration ne devrait pas suffire à convaincre les investisseurs que les choses iront prochainement dans le bon sens.
Nous déplorons également qu’il faille attendre jusqu’au 24 avril pour la publication des comptes annuels 2023. Une telle attente nous paraît interminable compte tenu du niveau de trésorerie actuel et des éventuels besoins du groupe pour financer son développement avant le lancement commercial de ses produits. En juin 2023, la trésorerie atteignait 5,3m€, sachant bien sûr que la consommation de cash de Crossject devrait se poursuivre pendant encore un (assez) long moment. Au S1 2023, le free cash flow représentait -8,3m€, avec 4,5m€ de capex. Dans ce contexte, la réaction très mesurée du marché (avec un titre à environ -20%) s’explique (en partie) par le fait que face à de nouveaux besoins en termes de financement, le groupe pourrait avoir recours à des instruments dilutifs. Si la direction affirme vouloir faire de son mieux pour éviter d’en arriver à une telle option, rien n’est certain. Compte tenu de l’évolution du titre, les investisseurs ne semblent pas convaincus que le groupe aura réellement le choix. Nous avons également de plus en plus de doutes sur la capacité du groupe à éviter une augmentation de capital ou tout autre instrument dilutif à l’horizon des prochains mois.
Enfin, le départ du directeur des opérations Engineering & Industry (qui en résumé chapeautait la production et le “supply”) a été annoncé. Il sera remplacé par le directeur industriel. Bien que dans fréquent dans la vie d’une entreprise, ce départ ne constitue pas non plus une bonne nouvelle.
Globalement, nous estimons que les investisseurs ont besoin de davantage d’éléments concrets pour être pleinement convaincus des perspectives offertes par le groupe. Même si des progrès ont été réalisés vers la commercialisation de Zeneo, il faudra beaucoup de temps avant que cette dernière ne porte ses fruits, ce qui laisse entrevoir d’autres mauvaises nouvelles sur le front du financement. D’autant plus que Crossject a depuis longtemps eu du mal à respecter les délais. Même en tenant compte des fonds récoltés grâce à l’accord signé avec la BARDA (3,2mUS$ en 2023) et au lease-back de l’immobilier sur plusieurs années, un recours au financement externe devrait s’imposer en 2024, et ce d’autant plus si l’obtention de l’EUA devait prendre plus de temps que prévu. Pour rappel, elle était attendue pour fin 2023/début 2024 et l’horloge tourne.
IMPACT
A ce stade, nous n’allons pas ajuster nos estimations/modèle dans l’attente de la publication des résultats 2023. Néanmoins, nous doutons un peu plus concernant le calendrier des lancements de produits sur le marché américain. S’il est certain que la direction n’a pas toutes les cartes en main en la matière, nous ne pouvons pas ignorer la perspective d’un nouveau recours au financement externe. De fait, nous prévoyons de réviser à la baisse de nos estimations (notamment en raison de rentrées de fonds plus tardives qu’anticipées), ce qui pourrait/devrait peser sur notre objectif de cours.
jamais attraper un couteau qui tombe !!!!
Prochain support 3.22
perso je viens dans reprendre
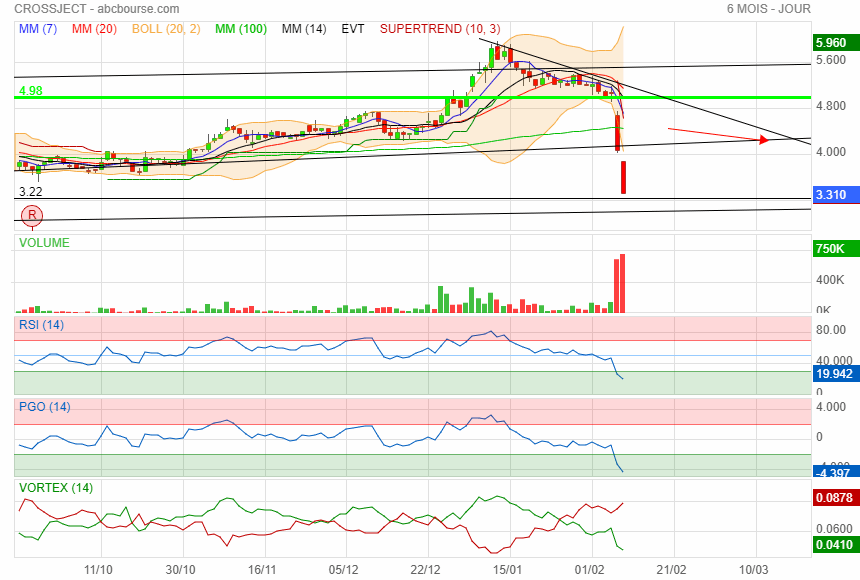
sauve qui peut ! c est peut être le bon moment dans reprendre
Crossject : la stratégie avance, mais la visibilité inquiète
Le 07 février 2024
Le titre Crossject évolue en forte baisse mercredi à la Bourse de Paris, les avancées dans son contrat décroché aux Etats-Unis ne suffisant pas à éclipser les inquiétudes entourant sa situation de trésorerie.
La société pharmaceutique, à l'origine d'un auto-injecteur sans aiguille qui permet de réaliser facilement des injections intramusculaires en situation d'urgence, a fait part hier soir d'une mise à jour stratégique pour 2024.
Sans surprise, l'entreprise compte accorder la priorité aux dépôts réglementaires et à l'accélération de ses efforts de commercialisation aux Etats-Unis.
Pour mémoire, Crossject a remporté auprès de l'Autorité américaine pour la R&D dans le domaine biomédical (BARDA) un contrat de 92 millions de dollars portant sur le développement d'un traitement d'urgence destiné à la prise en charge des crises épileptiques.
Dans son communiqué, la société souligne que ses discussions avec la FDA concernant les exigences nécessaires à l'autorisation d'urgence de Zepicure lui semblent 'en bonne voie'.
Selon les termes de l'accord avec la BARDA, Crossject a été remboursé au premier semestre 2023 de 3,2 millions de dollars au titre du développement réglementaire avancé américain.
La société a également obtenu un montant total d'environ cinq millions d'euros sur plusieurs années grâce à la cession-bail de plusieurs de ses bâtiments.
Les analystes d'Invest Securities jugent toutefois que 'la visibilité financière, sans premières livraisons à la BARDA, reste faible' selon leurs estimations.
A 14h15, l'action Crossject abandonnait 18,7%, après avoir chuté de plus de 20% à la mi-journée.
Crossject organisera un webcast le 6 février à 17h30 pour faire le point sur sa stratégie commerciale
Dijon, France, 1 février 2024 – 18 : 15 CET - Crossject (ISIN : FR0011716265 ; Euronext : ALCJ), une société pharmaceutique spécialisée qui développe des auto-injecteurs sans aiguille dédiés aux situations d’urgence, tiendra une conférence téléphonique en anglais sur sa stratégie commerciale aux États-Unis et en Europe le 6 février 2024 à 17h30 CET.
Patrick Alexandre, Président du Directoire de Crossject et Olivier Gire, Directeur Specialty Pharma, feront un point sur la stratégie commerciale de la Société à la suite de l'annonce du 4 janvier relative au partenariat stratégique avec Syneos Health, un leader entièrement intégré des services aux laboratoires biopharmaceutiques pour préparer le lancement commercial aux États-Unis de ZEPIZURE® le traitement innovant de secours de Crossject dans la prise en charge des crises épileptiques.
Le management de Crossject fera un point général sur ses activités et discutera des progrès accomplis par l'entreprise en ligne avec ses objectifs stratégiques.
Pour vous inscrire au webinaire, veuillez utiliser les détails suivants : https://us06web.zoom.us/webinar/register/WN_NcTN4As6R0i483uALLXFgw
L'enregistrement du webinaire sera disponible après l'événement.
Crossject : Oddo BHF engage le suivi
Les analystes d'ODDO BHF ont attribué à Crossject la recommandation 'Surperformance' avec un objectif de cours de 7,10 euros, faisant valoir les avantages considérables apportés par le dispositif sans aiguille Zeneo de l'entreprise, qui permet aux patients et aux soignants non formés d'administrer facilement des injections en une fraction de seconde dans des situations d'urgence.
Le contrat de Crossject avec l'Autorité américaine pour la R&D avancée dans le domaine biomédical (la BARDA) portant sur la fourniture de Zepizure, précédemment connu sous le nom de Zeneo Midazolam, dans le traitement des crises d'épilepsie causées par des agents neurotoxiques, constitue une validation importante de la plateforme d'après les analystes.
Cette nouvelle initiation complète la couverture de Crossject par les analystes d'Invest Securities et d'Alpha Value.
📈📈📈 Bientôt la question se posera : quand prendre ses bénéfices ❓❓❓
🫣
Crossject : Syneos Health engagé pour Zepizure aux Etats-Unis
Le 05 janvier 2024 à 09:00
Crossject annonce avoir engagé Syneos Health, groupe de services aux laboratoires biopharmaceutiques, pour la préparation au lancement commercial aux États-Unis du Zepizure, son traitement d'urgence innovant dans la prise en charge des crises d'épilepsie.
Dans le cadre de cet accord, Syneos Health apportera son soutien pour toutes les activités de pré-lancement et de lancement du produit, faisant bénéficier Crossject de sa présence aux États-Unis et son expertise dans la mise sur le marché de nouveaux traitements.
Pour l'instant tout ce passe bien
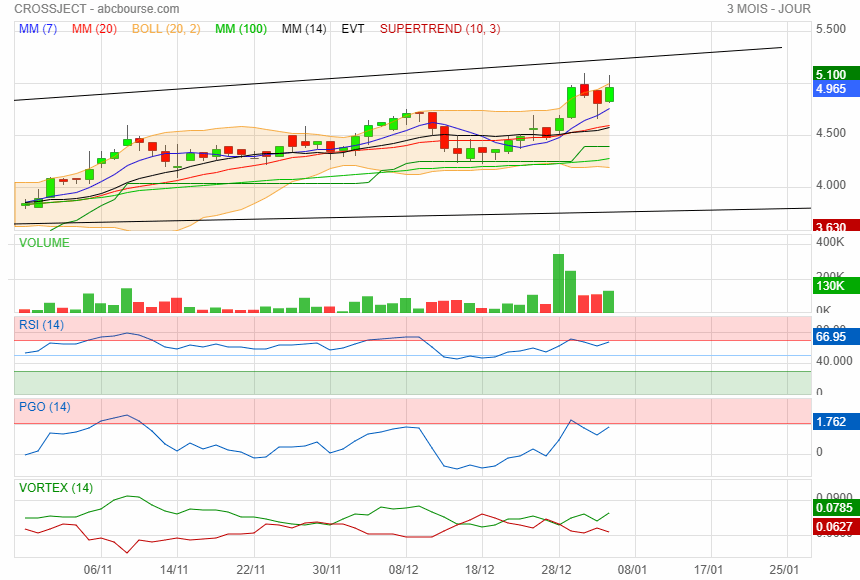
nette augmentation des volumes ces derniers jours
en moyenne plus de 100 000 titres/J et je ne tiens pas compte de l ordre de 190 000 titres échangés il y à 5 jours
à suivre ...
Crossject signe un nouvel accord de distribution en Europe du Nord
Le 03 janvier 2024 à 09:36
Au-delà de la commande ferme du BARDA (Biomedical Advanced Research and Development Authority) aux Etats-Unis et d’un accord de commercialisation pour l’Australie et la Nouvelle-Zélande, Crossject annonce avoir signé un accord de commercialisation en Europe du Nord pour ZEPIZURE (ex Midazolam). La nouvelle ne devrait pas avoir d’impact sur nos prévisions, ces dernières s’appuyant sur les produits effectivement lancés.
ACTUALITÉ
Crossject a annoncé la signature d’un accord de commercialisation en Europe du Nord pour ZEPIZURE (anciennement ZENEO Midazolam) couvrant l’Allemagne, le Royaume-Uni, le Danemark, la Suède, la Finlande et la Norvège.
ANALYSE
Même si le partenaire de cet accord n’a pas été communiqué et que, par conséquent, son envergure comme sa “puissance en termes de distribution” ne sont pas connues, il s’agit d’une bonne nouvelle pour le groupe français dont les produits seront accessibles à une population de 170m d’habitants. Sur le plan financier, Crossject percevra des paiements échelonnés pouvant représenter jusqu’à 1m€ en tout, une fois les autorisations de mise sur le marché obtenues dans les pays concernés par l’accord, ainsi qu’un pourcentage de la marge brute réalisée. Selon les termes de l’accord, Crossject assumera les coûts de développement réglementaire et détiendra toutes les autorisations de mise sur le marché qui en résulteront. Le partenaire supportera pour sa part les coûts commerciaux.
La nouvelle arrive après la commande ferme passée par la BARDA (Biomedical Advanced Research and Development Authority), et la signature de l’autre accord de commercialisation pour l’Australie et la Nouvelle-Zélande (avec AF Pharmaceuticals couvrant une population d’environ 30m d’habitants).
Ces deux accords et la commande passée aux États-Unis (BARDA) confirment que le groupe progresse vers la commercialisation de Zepizure et qu’il se met en ordre de marche en vue du lancement du produit dans ces régions une fois que les autorisations de mise sur le marché auront été obtenues.
IMPACT
La nouvelle ne devrait pas avoir d’impact nos prévisions, ces dernières s’appuyant sur les produits effectivement lancés. Comme pour les autres accords, le partenaire supportera une partie des coûts du groupe liés au développement et participera aux dépenses liées aux demandes de mise sur le marché.